震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚腈胺,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.已知三聚腈胺的化学式为C3H6N6
(1)三聚腈胺中氮的质量分数为______(保留两位小数,下同)
(2)蛋白质中含氮量平均为16%,某合格奶粉蛋白质含量为18%,则该奶粉含氮量为______某品牌奶粉1袋(400g)中加了1g三聚氰铵,相当于增加了______g蛋白质.
(3)三聚腈胺是一种重要化工原料,其主要用途有以下几方面:装饰面板、高档涂料、模塑粉、印钞用纸等,还可以作阻燃剂、减水剂、甲醛清洁剂等.自三聚腈胺事件后,许多人“谈化学物质色变”.请从“化学物质与人类社会的关系”角度,谈谈你对化学物质的认识(一句话即可)______.
【答案】
分析:(1)计算做出氮元素的质量分数
(2)要求三聚氰胺中氮元素的质量分数即为氮元素的质量比各元素的总质量.根据三聚氰胺的增加量先计算出氮元素的增加量,再根据蛋白质中氮元素的质量比计算出蛋白质的增加量.
(3)根据体会解答即可(答案可不唯一).
解答:解:(1)三聚氰胺的相对分子质量是12×3+14×6+1×6═126,其中氮的质量分数为
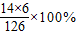
═66.7%;
故答案为:66.67%
(2)由题意可知:蛋白质含量为18%的奶粉中含氮量为16%×18%═2.88%;
1g三聚氰铵含氮元素的质量为1g×66.7%=0.667g,则相当于蛋白质的质量为0.667g÷16%=4.17g
故答案为:2.88%;4.17
(3)正确合理使用化学物质会造福人类,反之会带来灾害.
故答案为:化学物质对人类既包含有利的方面也包含有害的方面.
点评:本题主要考查元素质量比的计算,元素质量分数的计算以及化合物中某元素的质量计算,特别注重锻炼学生的思考及计算能力

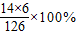 ═66.7%;
═66.7%;
