
| 实验内容 | 选用试剂或方法 | 反应的化学方程式或结论 |
| 鉴别H2和CO2 | 澄清石灰水 |
Ca(OH)2+CO2=CaCO3↓+H2O |
| 除去稀盐酸中混有的少量硫酸 | 氯化钡溶液 |
H2SO4+BaCl2=BaSO4↓+2HCl |
 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:
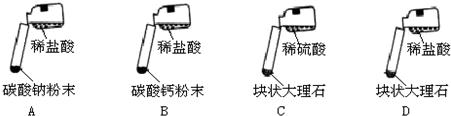

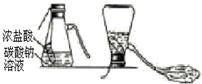 .
.查看答案和解析>>
科目:初中化学 来源: 题型:
| 操作 | 现象和结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 实验步骤 | 实验现象 | 实验结论 |
| 向B实验后的溶液中加入 稀盐酸(或氯化钙溶液等) 稀盐酸(或氯化钙溶液等) |
有气泡产生(或有白色沉淀生成等) 有气泡产生(或有白色沉淀生成等) |
验证了二氧化碳和氢氧化钠溶液反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
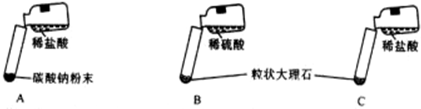
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率减慢,反应停止. | 无法持续产生CO2,不能用于实验室制CO2 |
| C | ① 产生大量气泡 产生大量气泡 |
② 反应速率适中,气体便于收集 反应速率适中,气体便于收集 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com