
实验员王老师要配制80g质量分数为10%的NaOH溶液供同学们使用,如图表示了他的实验操作过程。
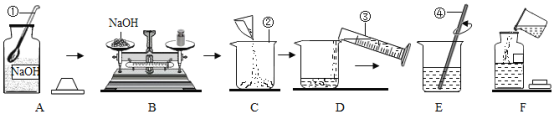
回答下列问题:
(1)写出仪器的名称①_____②_____
(2)B操作中有一处错误是_____,应称NaOH的质量是_____g,称量过程中若指针偏左,应进行的操作是_____。
(3)仪器③的规格应是_____(选填“50mL”或“100mL”),量取水时除仪器③外,还需要的一种仪器是_____。
(4)E操作中④的作用是_____。
(5)下列错误操作可能导致溶质的质量分数偏小的是_____(填序号)。
①B操作中砝码与NaOH放颠倒了(1g以下用游码)
②C操作中使用的烧杯内壁有水
③用量筒量水时仰视凹液面最低处读数
④F操作中溶液洒落
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:初中化学 来源:2020年江苏省扬州市(扬州教育学院附属中学)中考一模化学试卷 题型:流程题
某工厂产生的烧渣(主要含FeO、Fe2O3,还有一定量的SiO2)可用于制备绿矾(FeSO4·xH2O),工艺流程如下图所示::
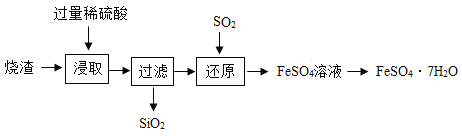
资料1: SiO2不溶于水,也不与稀硫酸反应;
资料2: +2价的铁元素容易被空气中的氧气氧化。
(1)“浸取”步骤中,FeO、Fe2O3和稀硫酸发生反应的化学方程式为:FeO+ H2SO4= FeSO4+ H2O、_________,为提高“浸取”步骤的反应速率,除了采取“搅拌”和“使用催化剂”外,还可采取的具体措施有________(写1条)。
(2)“浸取”、“过滤”步骤后,滤液中的溶质有_________。
(3)“还原”转化的化学反应原理为:SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4,该步骤的主要目的是______。
(4)FeSO4溶液经过蒸发浓缩、______________、过滤、洗涤、低温干燥后得到FeSO4·xH2O晶体;低温干燥的目的是______________。
(5)以上结晶过程最好在氮气环境中进行,氮气的作用是___________。
查看答案和解析>>
科目:初中化学 来源:2020年重庆市中考二模化学试卷 题型:单选题
如图所示,鱼、肉的新鲜度不同,其浸出液pH会发生相应变化。鱼、肉的浸出液来判它们新鲜度,下列说法错误的是( )
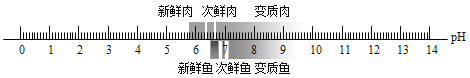
A.鱼肉的浸出液pH变大越趋向腐败变质
B.新鲜鱼肉漫出液比次鲜鱼肉的pH小,新鲜鱼肉浸出液比次鲜鱼肉酸性弱
C.新鲜鱼肉浸出液为酸性,能与活泼金属单质反应
D.变质鱼肉浸出液能使无色酚酞变红
查看答案和解析>>
科目:初中化学 来源:四川省成都市2019-2020学年九年级上学期12月月考化学试卷 题型:单选题
将X克的氯酸钾和Y克的二氧化锰的混合物加热至完全反应,可得到Z克的氯化钾。根据质量守恒定律,该反应得到的氧气质量为
A.X-Y B.X+Y-Z C.X-Z D.X+Y+Z
查看答案和解析>>
科目:初中化学 来源:四川省成都市2019-2020学年九年级上学期12月月考化学试卷 题型:单选题
下列关于碳的几种单质的组成和用途的说法,错误的是
A.璀灿夺目的天然钻石是由碳元素组成的
B.长期未用而难开启的铁锁,可在锁孔中加入少量铅笔芯粉未作润滑剂
C.铅笔芯主要是用铅和少量石墨粉制成的
D.活性炭可用作防毒面具的滤毒剂
查看答案和解析>>
科目:初中化学 来源:2020年山东省潍坊市昌邑市、诸城市中考一模化学试卷 题型:计算题
某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图像如下:

次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 | 50 |
烧杯中物质的质量/g | 100 | 150 | 197.8 | 245.6 | 295.6 |
请根据有关信息计算:
(1)a的数值为________。
(2)稀盐酸中溶质的质量分数为_____。(写出计算过程)
(3)恰好完全反应后所得溶液中溶质的质量为_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源:2020年山东省潍坊市昌邑市、诸城市中考一模化学试卷 题型:单选题
“化学链燃烧”技术是目前能源领域研究的热点之一。氧化镍(NiO)作载氧体的“化学链燃烧”过程如图所示:
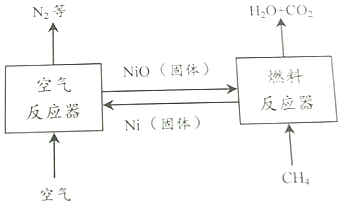
相比直接燃烧甲烷,对该技术的评价错误的是( )
A. 能量损耗少、利用率高
B. 较安全,减少爆炸风险
C. 消耗等质量甲烷,参加反应氧气较少
D. 有利于分离和回收较纯净的二氧化碳
查看答案和解析>>
科目:初中化学 来源:2020年山东省潍坊市诸城市中考一模化学试卷 题型:流程题
工业上利用某废渣(含FeSO4、Fe2(SO4)3及少量CaO和MgO)制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4,其生产流程如下:

已知:a、氧化还原反应中,会有元素化合价发生变化。
b、 回答下列问题:
回答下列问题:
(1)(NH4)2Fe6(SO4)4(OH)12中铁元素的化合价是_____。
(2)粉碎废渣的目的_____,加入物质X溶解废渣,X应选用_____(填序号)。
A 盐酸
B 硫酸
C 氨水
D 氢氧化钠
步骤①酸浸时,生成盐的化学方程式为_____(任写一个)。
(3)步骤③中操作Y的名称是____,滤液中除含有很少量铵黄铁矾外还含有__。
(4)步骤②通入氧气氧化的目的是_____,工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe3+氧化率的变化规律:_____。

查看答案和解析>>
科目:初中化学 来源:山东省泰安市岱岳区2019-2020学年八年级下学期期中化学试卷 题型:单选题
下列物质的用途有错误的是
A.氧气有助燃性,可做燃料 B.自来水可用于灭火
C.氮气充入食品包装袋内防腐 D.稀有气体充入灯泡中可使其耐用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com