
【题目】为了测定金属镁样品中镁的质量分数(杂质不含镁元素,不溶于水,也不与其它物质发生反应),进行了如下实验:请回答下列问题:
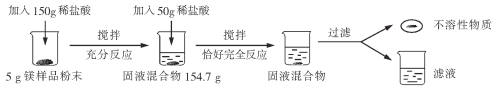
(1)上述实验过程中发生反应的化学方程式为________________________________。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式________________。
(3)此镁样品中镁的质量分数为________________。
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为________________。
(5)若将反应后的滤液蒸发104.4g水,无晶体析出,所得溶液中溶质的质量分数为__________。
(6)若要生产含镁4.5%的铝合金960t,需要上述金属镁样品的质量为________________。
【答案】Mg+2HCl=MgCl2+H2↑ ![]() 96% 40g 19% 45t
96% 40g 19% 45t
【解析】
(1)实验过程中发生反应是镁和盐酸反应生成氯化镁和氢气,对应的化学方程式为 Mg+2HCl=MgCl2+H2↑。
(2)由于所加盐酸为同一盐酸,且根据第一次150g稀盐酸完全反应生成氢气为0.3g,所以继续加入50g稀盐酸恰好完全反应,则生成的氢气的质量总量为0.4g
第一次所加的稀盐酸中溶质质量为x
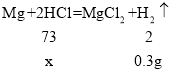
![]()
(3)设镁样品中镁的质量分数为y,消耗的盐酸的质量分数为z,生成的氯化镁的质量为a
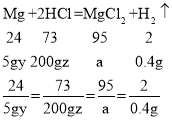
![]()
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为![]()
(5)若将反应后的滤液蒸发104.4g水,无晶体析出,所得溶液中溶质的质量分数为![]()
(6)若要生产含镁4.5%的铝合金960t,需要上述金属镁样品的质量为![]()
故答案为:
(1)Mg+2HCl=MgCl2+H2↑。
(2)![]() 。
。
(3)96%。
(4)40g。
(5)19%。
(6)45t。


科目:初中化学 来源: 题型:
【题目】对下列化学用语中数字“2”含义的说法正确的是( )
①2H ②2NH3 ③SO2 ④![]() ⑤Mg2+ ⑥2OH- ⑦H2O
⑤Mg2+ ⑥2OH- ⑦H2O
A. 表示离子个数的是⑤⑥B. 表示分子中原子个数的是③⑦
C. 表示离子所带电荷数的是④⑤D. 表示分子个数的是①②
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】H2O2可作增氧剂。常温下,用4%H2O2溶液进行实验,研究pH对H2O2分解所得溶液中氧量的影响,测定结果如图。

(1)H2O2分解的化学方程式为____________________。
(2)分析如图得到的结论是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年10月,中国女科学家屠呦呦获得了2015年诺贝尔生理学或医学奖。她所研究的青蒿素的化学式是C15H22O5,该物质的摩尔质量是_____;该物质中碳元素的质量分数是_____(精确到0.1%);该物质的分子中碳、氢、氧原子的物质的量之比是_____;2摩尔该物质的分子中有_____个氧原子。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】少年强则国强,科技兴则国兴。北斗组网、嫦娥探月、蚊龙潜海、磁浮(高铁)纵横……,中国科技的迅猛发展一次又一次让世界见证“中国速度” !

(1)火箭、卫星、船舶等制造业常使用玻璃钢、塑料、钛合金等材料,其中玻璃钢属于____________(填字母)。
A 金属材料 B 复合材料 C 有机高分子材料
(2)钛和钛合金是21世纪重要的金属材料,有很多优良的性能, 如____________(填字母)。
A 熔点低、易加工B 密度大、强度好 C 机械性能好、抗腐蚀性好
(3)潜水器中的微型电子仪器常用银锌电池作电源,在放电时可把氧化银转化成银,则放电时银元素的化合价变化为____________,放电时的能量转化是____________能转化为____________能。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有下列5种粒子的结构示意图。
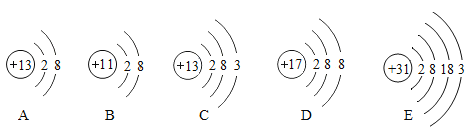
回答下列问题
(1)以上示意图中,共有________种元素;
(2)A粒子中的质子数为________ ;
(3)上述5种粒子中,最外层电子数相同的原子是________ ;
(4)B粒子与D粒子形成的化合物化学式是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】抛撒融雪剂和消融路面积雪,研究人员配制出A、B两组融雪剂,组成成分及质量分数如下表
A组 | B组 |
CH3COOK 36% KHPO414% CaC12 14% MgC12 36% | CH3COOK 40% KH2PO4 14% CaC12 15% KHCO3 31% |
回答下列问题
(1)A、B两组融雪剂相比较,________组的CH3COOK(乙酸钾)含量高
(2)KH2PO4的相对分子质量为__________
(3)B组融雪剂中,含氯的质量分数为__________(填计算结果)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜矿(主要成分是CuFeS2)经初步处理后,所得溶液甲中溶质为Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示[Fe2(SO4)3+Fe═3FeSO4]:
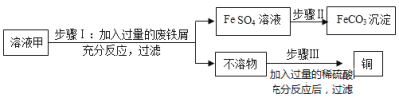

图1 图2
(1)步骤Ⅰ加入的废铁屑中含有少量铁锈,但对产物的成分没有影响,原因是_____.
(2)步骤Ⅱ中加入一种可溶性试剂可实现其转化,该试剂可以是_____。
(3)为了测定步骤Ⅲ中所用稀硫酸的溶质质量分数,该同学取两份相同溶质质量分数的稀硫酸各100g,分别加入等质量的铁和锌,相同条件下充分反应,产生氢气的质量随时间变化的曲线如图2所示,则下列说法正确的是_____。
A 表示锌和稀硫酸反应的情况的是曲线a
B 稀硫酸的溶质质量分数为9.8%
C 加入铁的质量至少有5.6g
D 加入锌的质量可能是13g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C、D四种固体物质的溶解度曲线,根据读图,填空:
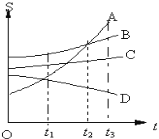
⑴t1℃时,四种物质溶解度由大到小的顺序是_____。
⑵t3℃时,分别将四种物质的等质量的饱和溶液降温至t1℃,其中,析出溶质的质量最多的是_____,溶液呈不饱和状态的物质是_____。
⑶A、B两种物质的溶解度相等时的温度是_____。
⑷A中含少量C时,可以用_____法提纯A。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com