
科目:初中化学 来源:化学教研室 题型:022
查看答案和解析>>
科目:初中化学 来源: 题型:
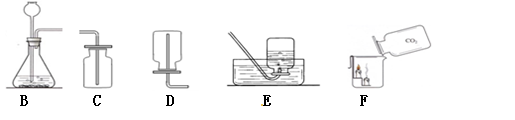
 ),反应的化学方程式为 。
),反应的化学方程式为 。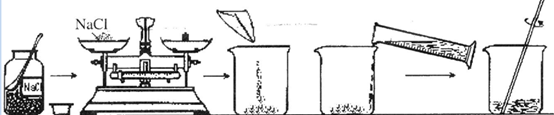 取食盐的过程中,发现指针偏向分度盘右侧,
取食盐的过程中,发现指针偏向分度盘右侧,| A.在左盘上减少氯化钠,直至天平平衡 | B.在右盘上减少砝码,直至天平平衡 |
| C.在左盘上继续增加氯化钠,直至天平平衡 | D.移动游码,直至天平平衡 |
查看答案和解析>>
科目:初中化学 来源:2012届福建省龙岩市上杭县九年级化学总复习试卷(二) 题型:填空题
2005年10月14日,龙岩市南城后孟路段发生一起装浓硫酸的运输车因驾驶不慎,造成浓硫酸大面积泄漏事故。请回答下列问题:
⑴实验室用浓硫酸(溶质质量分数为98%,密度为1.84gcm-3)配制300g溶质质量分数11%的稀硫酸。(结果保留一位小数)
a、计算:需浓硫酸 ml 水 ml
b、量取:用规格为 ml的量筒量取浓硫酸(1.50ml、100ml)中选择
用量筒量取水
c、稀释:稀释浓硫酸时一定要把 慢慢注入 中并不断搅拌
⑵下列物质暴露在空气中会变质的是
A、浓硫酸 B、浓盐酸 C、烧碱 D、木炭
⑶在Fe、Cu、HCl、Ca(OH)2、Fe2O3,纯碱、烧碱中不能与H2SO4发生化学反应的有
(填化学式)
写出其中一个化学反应方程式 。
⑷为使事故对环境造成的影响尽可能降低,下列措施中最佳措施为
A、用大量水冲洗 B、撒熟石灰 C、撒沙土 D、撒烧碱
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.
铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.| 配置用水 | 有浑浊 | 有浑浊 |
| 自来水 | 无浑浊 | 有浑浊 |
| 市售纯净水 | 无浑浊 | 有浑浊 |
| 医用纯净水 | 无浑浊 | 无浑浊 |
| 试验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 饱和溶液 | 2 | 4 | 6 | 8 | 16 | 32 | 128 |
| 现 象 | 白色浑浊→澄清 | ||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com