
| A. | 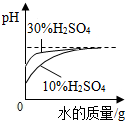 稀释等质量溶质质量分数分别为30%和10%的H2SO4溶液 | |
| B. | 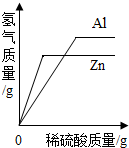 等质量的Al、Zn与足量的等溶质质量分数的稀硫酸反应 | |
| C. | 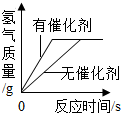 用等质量、等容质质量分数的过氧化氢溶液分别制取氧气 | |
| D. | 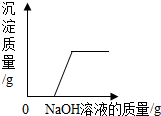 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液 |
分析 A、根据稀释H2SO4溶液,溶液的pH值只能无限的接近于7判断;
B、根据金属的活动性以及反应后产生气体的质量大小来分析;
C、根据催化剂只是改变反应的速率,与生成的产物多少无关判断;
D、根据氯化铜、硝酸铜和氢氧化钠反应都生成氢氧化铜沉淀分析.
解答 解:
A、稀释H2SO4溶液,溶液的pH值只能无限的接近于7,但30%的H2SO4溶液的pH应小于110%的H2SO4溶液,故错误.
B、等质量的锌和铝与足量的稀硫酸反应,铝产生的氢气多,铝的活动性大于锌,故铝最先反应结束,故错误;
C、催化剂只是改变反应的速率,与生成的产物多少无关,故正确;
D、氯化铜和氢氧化钠反应生成氢氧化铜沉淀,硝酸铜和氢氧化钠反应生成氢氧化铜沉淀,所以沉淀从零开始,直至反应结束不再增长,故错误;
答案:C
点评 本题通过图象的形式考查了常见物质的性质,正确辨别坐标所表示的意义及坐标所表示的量的关系是解决问题的关键.此题是化学反应与图象知识的考查题,结合反应的过程与图象情况的走势联系起来是解题的关键所在.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:解答题
 我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.
我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.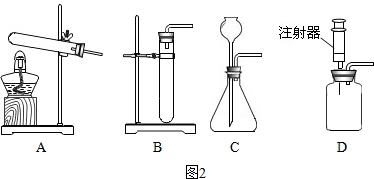
| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均20mL | 每次用量均5g |
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和④探究温度对反应快慢的影响; (III)实验①和③③探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | 10% | |
| ③ | 20℃ | 细颗粒 | 5% | |
| ④ | 40℃ | 粗颗粒 | 10% |
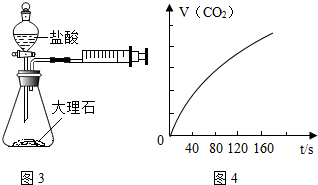 实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.
实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
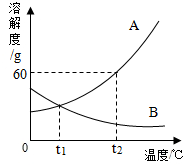 如图是A、B固体物质的溶解度曲线
如图是A、B固体物质的溶解度曲线查看答案和解析>>
科目:初中化学 来源: 题型:解答题
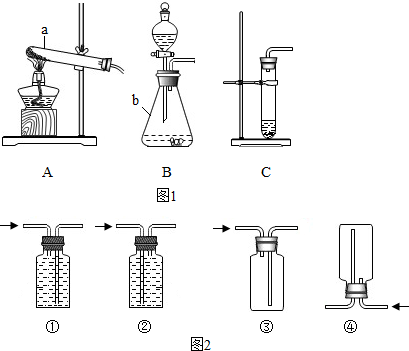
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁在潮湿的空气中容易生锈 | B. | 大理石、金刚石都是无机材料 | ||
| C. | 铝合金比铝的强度和硬度高 | D. | 合金、合成纤维都是有机合成材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com