
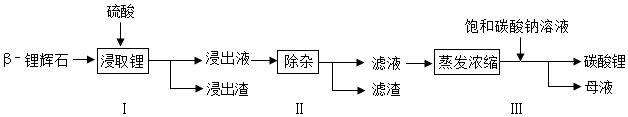
分析 (1)反应物接触越充分,反应速率越快;
(2)碳酸钙能和酸性物质反应;
(3)H2O2溶液能把亚铁离子氧化成铁离子,石灰乳中的氢氧化钙能和镁离子反应生成氢氧化镁沉淀,碳酸根离子能和钙离子结合成碳酸钙沉淀;
(4)根据反应情况可以判断从母液中可回收的主要物质.
解答 解:(1)步骤I前,β-锂辉石要粉碎成细颗粒的目的是增加接触面积,使反应充分,同时加快反应速率.
故填:增加接触面积,使反应充分,同时加快反应速率.
(2)步骤I中,酸浸后得到的酸性溶液除含有Li+、SO42-,还含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石,这是因为石灰石中的碳酸钙能和酸浸后得到的酸性溶液反应,以调节溶液的pH到6.0~6.5.
故填:石灰石.
(3)步骤II中,H2O2溶液能把亚铁离子氧化成铁离子,石灰乳中的氢氧化钙能和镁离子反应生成氢氧化镁沉淀,碳酸根离子能和钙离子结合成碳酸钙沉淀,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有Fe2+、Mg2+、Ca2+.
故填:Fe2+、Mg2+、Ca2+.
(4)从母液中可回收的主要物质是硫酸锂和碳酸钠反应生成的硫酸钠,氢氧根离子和钠离子结合成的氢氧化钠.
故填:NaOH、Na2SO4.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、化学与生活 | B、化学与安全 |
| ①用洗涤剂去除油污 ②用醋酸除水垢 ③用食盐除公路上的积雪 | ①炒菜锅着火可以用锅盖盖火 ②在室内放一盆水能防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 |
| C、化学与资源 | D、化学与发现 |
| ①防止金属腐蚀是保护金属资源的途径之一 ②煤、石油、天然气是可再生能源 ③海洋中蕴藏着丰富的化学资源 | ①波义耳发现酸碱指示剂 ②拉瓦锡发现元素周期律并编制元素周期表 ③门捷列夫发现空气的组成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
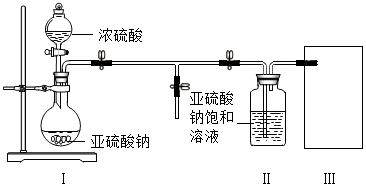
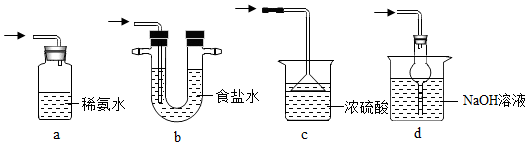
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
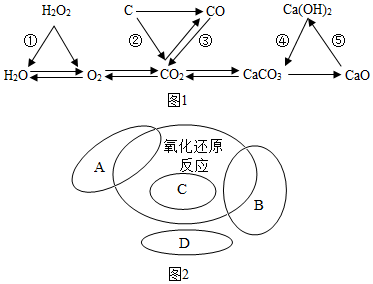
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 茶树不宜在碱性土壤中生长 | |
| C. | 一个茶氨酸分子中含有3个氧原子 | |
| D. | 茶叶中的锌、硒指单质,茶氨酸属于有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com