
 黄铜是铜和锌的合金(Cu-Zn).某同学为了测定某黄铜屑样品的组成,取四份样品,分别加入一定量的稀硫酸,反应后测得其实验数据记录如下表.
黄铜是铜和锌的合金(Cu-Zn).某同学为了测定某黄铜屑样品的组成,取四份样品,分别加入一定量的稀硫酸,反应后测得其实验数据记录如下表.| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品的质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 加稀硫酸的质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体的质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
分析 根据金属与酸反应的条件可知,锌与酸反应,铜与酸不反应.再由表中数据分析可知,第三次反应是合金中的锌反应完了,前两次是酸完全反应,合金有剩余,再正确写出方程式,由方程式求出锌的质量,就可以求得黄铜中锌的质量分数,据此分析解答.
解答 解:根据第2份样品的反应数据可知,加入80g稀硫酸时,产生氢气质量增加,说明第1份样品与40g稀硫酸并未能完全反应,金属样品有剩余,所以40g硫酸完全反应会生成0.4g氢气,由第三份样品反应的情况看生成的氢气是1g,所以可知硫酸未反应完,即50g样品完全反应会生成1.0g氢气;
(1)在第1份样品测得的数据中,稀硫酸完全反应了.
(2)设原混合物中含锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 1.0g
$\frac{65}{x}=\frac{2}{1.0g}$
x=32.5g
∴黄铜屑样品中的锌的质量分数=$\frac{32.5g}{50g}$×100%=65%
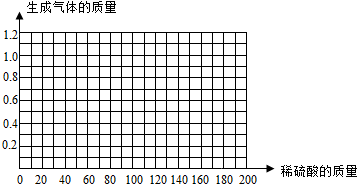
(3)当没有硫酸加入时,就没有气体的放出,因此起点是(0,0);比较第一份和第二份可以发现,每加入40克硫酸,气体就会多放出0.4克,因此要想放出1.0克气体,需要加入硫酸的质量是100克,因此最高点是(100,1.0);比较第一份和第二份可以发现,硫酸的质量和气体的质量的比值相等(斜率相同),所以图象是一条直线.
答案:
(1)稀硫酸
(2)黄铜屑样品中的锌的质量分数65%
(3)
点评 本题考查了学生对图表中数据的分析能力,完成此题可以依据金属与酸的反应以及进行情况的分析探讨,要学会分析表格中的数据是解题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
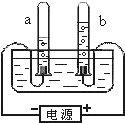 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 白磷 | 红磷 | 木炭 | 无烟煤 |
| 着火点/℃ | 40 | 240 | 320-370 | 700-750 |
| A. | 白磷、红磷、木材、酒精都是可燃物 | |
| B. | 降低可燃物的着火点可以达到灭火的目的 | |
| C. | 实验时,用于吸干白磷的滤纸片不能丢在废纸篓里 | |
| D. | 红磷燃烧属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
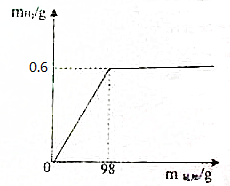 某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金40g,加入足量的稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示的曲线图,回答下列问题:
某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金40g,加入足量的稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示的曲线图,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 组别 | ① | ② | ③ | ④ |
| 溶液中FeCl3的质量(g) | 65 | 65 | 65 | 65 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
| A. | 第①组:反应后溶液中含有32.5克FeCl3 | |
| B. | 第②组:在反应后溶液中放入一根铁丝,铁钉表面无变化 | |
| C. | 第③组:剩余固体中滴加盐酸无气泡产生 | |
| D. | 第④组:剩余固体中铁与铜的物质的量之比为1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com