
| 实验序号 | 实验1 | 实验2 | 实验3 |
方案 | 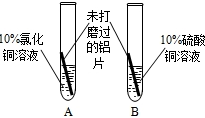 | 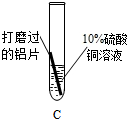 | 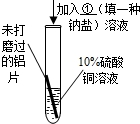 ① |
现象 | A中铝片表面有红色固体析出;B中铝片无明显现象. | 与A中的现象相 | |
结论 | 溶液中对氧化膜产生了破坏作用的离子可能是 | 除去表面氧化膜的铝片会与CuSO4溶液反应.该反应的化学方程式 | 验证了实验1的结论. |
| 54 |
| x |
| 6 |
| 4g+100g-103.7g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
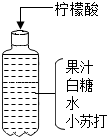 小华按如图配方自制了一瓶清凉甘甜的汽水.根据图中信息回答:
小华按如图配方自制了一瓶清凉甘甜的汽水.根据图中信息回答:查看答案和解析>>
科目:初中化学 来源: 题型:
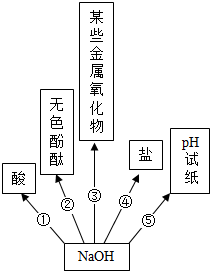 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:| 实验操作 | 化学方程式 |
| ① | CuCl2+Fe═Cu+FeCl2 |
| ②过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
| 1 |
| 3 |
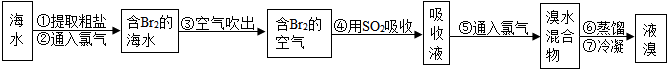
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com