
| 该元素的相对原子质量×该元素的原子个数 |
| 化合物的相对原子质量 |
| 该纯净物的质量 |
| 混合物的质量 |
| 混合物中某元素的质量分数 |
| 纯净物中某元素的质量分数 |
| N的相对原子质量×N的原子个数 |
| (NH4)2SO4的相对分子质量 |
| 28 |
| 132 |
| 18.9% |
| 21.2% |
| 混合物中某元素的质量分数 |
| 纯净物中某元素的质量分数 |


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:初中化学 来源: 题型:
 (2005?包头)甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸.甲试管内产生的现象是
(2005?包头)甲、乙两种固体物质的溶解度曲线如图所示.现将两支分别装有甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有水的烧杯里,然后向烧杯中加入一定量的浓硫酸.甲试管内产生的现象是查看答案和解析>>
科目:初中化学 来源: 题型:
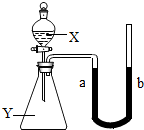 (2005?包头)如图所示,锥形瓶内盛有物质Y(可能为气体、溶液或固体),分液漏斗内盛有液体X,U形管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时.回答下列问题:
(2005?包头)如图所示,锥形瓶内盛有物质Y(可能为气体、溶液或固体),分液漏斗内盛有液体X,U形管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴入锥形瓶内时.回答下列问题:查看答案和解析>>
科目:初中化学 来源:2007年陕西省中考化学预测试卷(五)(解析版) 题型:选择题
 3Cu+A12O3.反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中.下列叙述的现象中,能够说明氧化铜没有完全反应的是( )
3Cu+A12O3.反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中.下列叙述的现象中,能够说明氧化铜没有完全反应的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com