
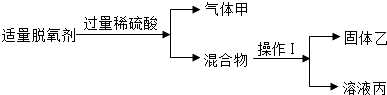
分析 (1)根据物质的化学式可以读出物质的名称,根据化学方程式可以判断反应类型;
(2)实验Ⅰ:
①过滤可以把不溶于水的物质除去,活性炭具有吸附性,常常用作吸附剂;
②根据铁与硫酸反应,生成硫酸亚铁和氢气解答;
③根据反应过程可以判断溶液中的溶质.
解答 解:(1)Fe(OH)2读作氢氧化亚铁;此反应中,反应物是多种,生成物是一种,属于化合反应;
(2)实验Ⅰ:
①操作Ⅰ的名称是过滤,乙在净水中用作是吸附剂;
②铁与硫酸反应,生成硫酸亚铁和氢气,发生反应的化学方程式为:Fe+H2SO4═FeO4+H2↑;
③溶液丙中含有的溶质有:反应生成的硫酸亚铁,原来的氯化钠,还有没有反应的硫酸;
故答案为:(1)氢氧化亚铁,化合反应;
(2)①过滤,吸附剂;
②Fe+H2SO4═FeO4+H2↑;
③FeSO4、NaCl、H2SO4;
点评 本题主要考查实验探究方面的知识,解答时要掌握物质之间相互作用时的反应情况,特别是要能够根据物质的性质方面的知识来判断具体的物质,并且能够根据质量守恒定律的内容正确的书写反应的化学方程式.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定含有Ag、Cu和Fe | |
| B. | 滤渣中一定有Ag,可能含有Cu,一定不含Fe | |
| C. | 滤液中一定有AgNO3、Zn(NO3)2,一定没有Cu(NO3)2 | |
| D. | 滤液中一定没有AgNO3、Cu(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界中的水都属于化合物,溶液都属于混合物 | |
| B. | 硬水和软水都属于溶液,生活中可通过加热的方法将硬水软化 | |
| C. | 溶液中的溶剂不一定是水,硫酸铜溶液中溶剂是硫酸 | |
| D. | 某物质在100g溶剂里达到饱和状态时所溶解的质量就是该物质的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
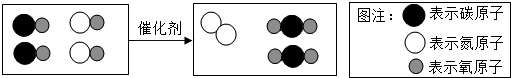
 ”和“
”和“ ”分别表示两种不同的原子.由粒子甲“
”分别表示两种不同的原子.由粒子甲“ ”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为2:1,此反应的基本反应类型为化合反应.任举一例符合此反应类型的化学方程式:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
”聚集成的物质可能(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为2:1,此反应的基本反应类型为化合反应.任举一例符合此反应类型的化学方程式:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为了治疗胃酸过多,可以遵循医嘱服用某些碱性的物质,如:氢氧化铝、氢氧化钠 | |
| B. | 工业用盐如亚硝酸钠具有咸味,可以代替食盐用于生活烹调 | |
| C. | 在海水中加入活性炭可以淡化海水 | |
| D. | 在食用皮蛋时可以蘸点食醋,以中和皮蛋中含有的少量碱性物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁制品的表面生锈后不必立即清除,理由是铁锈能阻止内部的铁继续生锈 | |
| B. | 铝锅用久了表面会有些污垢,最科学的除去污垢的方法是用钢丝球用力擦洗 | |
| C. | 铝制品具有较强的耐腐蚀性,其原因是铝的化学性质不活泼,盛醋最好选择铝制容器 | |
| D. | “暖宝宝”中有铁粉、氯化钠和水等,发热原理是铁粉氧化放热,“暖宝宝”应密封保存 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 加热前质量(g) | 加热后质量(g) | |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应前后分子数目改变 | B. | 反应前后元素种类不变 | ||
| C. | 反应前后的质量比为45:16 | D. | 反应前后氮元素化合价发生改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com