
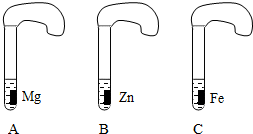
 一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图所示):
一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图所示):分析 为了探究金属Mg、Zn、Fe与酸反应的快慢,需要控制酸、金属及操作等可变量,酸应使用质量分数相同、质量相同的同一种酸,金属应取大小相同、外观一致的金属,操作时应同时加入、相同的气球也应同时套在试管口上;根据金属与的酸反应分析相同质量的三种金属与足量的稀盐酸反应,生成氢气的质量的多少.
解答 解:(1)锌与盐酸反应,生成氯化锌和氢气;反应的化学方程式是:Zn+2HCl$\frac{\underline{\;点燃\;}}{\;}$ZnCl2+H2↑
(2)三种金属中,镁的活动性最强,放出氢气速率最大,所以放入镁的A试管气球膨胀速度最快;
(3)实验室制取气体时要求反应速度不能太快,反应太剧烈不宜于控制;也不能反应速度太慢,太慢收集需要太长时间;镁与酸反应太快、铁反应速度太慢,实验室制取氢气时不选用这两种金属;
(4)镁的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成$\frac{1}{12}$克氢气.
锌的相对原子质量为65,65g锌可反应生成2g氢气,即1g锌生$\frac{1}{32.5}$克氢气.
铁的相对原子质量56,56g铁可反应生成2g氢气,即1g铁生成$\frac{1}{28}$克氢气.
因为$\frac{1}{12}$>$\frac{1}{28}$>$\frac{1}{32.5}$,所以镁放出的氢气最多.
故答为:(1)Zn+2HCl$\frac{\underline{\;点燃\;}}{\;}$ZnCl2+H2↑; (2)A;(3)镁的反应速度太快不易收集,铁的反应慢收集时间过长. (4)Mg.根据选项中元素的相对原子质量和它们与稀盐酸反应的化学方程式,计算出1g这些金属分别与足量稀盐酸反应生成氢气的质量,再进行比较即可.
点评 实验室制取氢气通常选择锌粒与稀硫酸反应,一般选择稀硫酸而不选择稀盐酸是由于稀硫酸没有挥发性而盐酸有挥发性.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com