
ijŹµŃ銔×éČ”Ņ»¶ØĮæµÄĀČĖį¼ŲŗĶ¶žŃõ»ÆĆĢ»ģŗĻŗóÖĘŃõĘų£¬³ä·Ö·“Ó¦ŗó½«ŹµŃéŹ£Óą¹ĢĢå25.4g¼ÓČėÉÕ±ÖŠ£¬ĻņÉÕ±ÖŠ¼ÓČė×ćĮæµÄĖ®²¢³ä·Ö½Į°č£¬ŌŁĻņÉÕ±ÖŠµĪ¼Ó×ćĮæĻõĖįŅųČÜŅŗ£¬·“Ó¦ŗó¹żĀĖ”¢Ļ“µÓ”¢øÉŌļµĆµ½¹ĢĢå39.2g£¬ŌņŌ»ģŗĻĪļÖŠĀČĖį¼ŲµÄŗ¬ĮæĪŖ£Ø £©
A. 50% B. 70% C. 80% D. 98%
B ”¾½āĪö”æÉčŌ»ģŗĻĪļÖŠĀČĖį¼ŲµÄÖŹĮæĪŖ£¬Éś³ÉĀČ»Æ¼ŲµÄÖŹĮæĪŖy£¬ KCl+AgNO3ØTKNO3+AgCl”ż ¹ĢĢåÖŹĮæ²īĮæ=143.5-74.5=69 ÓÉ2KClO32KCl+3O2”ü”¢KCl+AgNO3ØTKNO3+AgCl”ż£¬æÉµĆ£ŗ ŌņKClO3”«KCl”«AgCl 122.5 74.5¹ĢĢåÖŹĮæ²īĮæ=69 ... Ķ¬²½Į·Ļ°Ēæ»ÆĶŲÕ¹ĻµĮŠ“š°ø
Ķ¬²½Į·Ļ°Ēæ»ÆĶŲÕ¹ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ°²»ÕŹ”ÄĻĮźĻŲ2018½ģ¾ÅÄź¼¶ĻĀѧʌµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
Ė®ŹĒÉśĆüÖ®Ō“”£ĻĀĮŠÓŠ¹ŲĖ®µÄĖµ·Ø“ķĪóµÄŹĒ
A. Ė®ÓÉĒāŌ×ÓŗĶŃõŌ×Ó¹¹³É B. Éś»īÖŠĶعżÖó·ŠæÉŅŌ½µµĶĖ®µÄÓ²¶Č
C. æÉÓĆ·ŹŌķĖ®Ēų·ÖÓ²Ė®ŗĶČķĖ® D. Ė®ŌŚĶصēĢõ¼žĻĀ·Ö½ā³ÉĒāĘųŗĶŃõĘų
A ”¾½āĪö”æŹŌĢā·ÖĪö£ŗĖ®·Ö×ÓÓÉĒāŌ×ÓŗĶŃõŌ×Ó¹¹³É£»Éś»īÖŠĶعżÖó·ŠæÉŅŌ½µµĶĖ®µÄÓ²¶Č£»æÉÓĆ·ŹŌķĖ®Ēų·ÖÓ²Ė®ŗĶČķĖ®£»Ė®ŌŚĶصēĢõ¼žĻĀ·Ö½ā³ÉĒāĘųŗĶŃõĘų”£¹ŹŃ”£Į£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗž±±Ź”»ĘŹÆŹŠ2018½ģ¾ÅÄź¼¶3ŌĀŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ŗīŹĻÖĘ¼ī·ØÖŠµÄ”°¼ī”±______£»
A. Š”ĖÕ“ņ B. Ć÷·Æ C. “æ¼ī D. ŹģŹÆ»Ņ”£
C ”¾½āĪö”æŗīŹĻÖĘ¼ī·ØÖŠµÄ”°¼ī”±ŹĒ“æ¼ī£¬Ģ¼ĖįÄĘ”£ µć¾¦”ĆŗņµĀ°īĮŖŗĻÖĘ¼ī·Ø¾ĶŹĒĪŖĮĖÖĘČ”“æ¼ī”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ĪŽĪżŹŠ¶”ŹńѧĒų2018½ģ¾ÅÄź¼¶ĻĀѧʌµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
”°84Ļū¶¾Ņŗ”±µÄÓŠŠ§³É·ÖĪŖ“ĪĀČĖįÄĘNaClO£¬ĘäÖŠĀČŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ
A. +1 B. +3 C. +5 D. -1
A ”¾½āĪö”æ“ĪĀČĖįÄĘ£ØNaClO£©ÖŠÄĘĪŖ+1¼Ū£¬ŃõĪŖ-2¼Ū£¬»ÆŗĻĪļÖŠÕżøŗ»ÆŗĻ¼Ū“śŹżŗĶĪŖĮć”£Éč£ŗĀČŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖx£¬Ōņ£ŗ£Ø+1£©+x+£Ø-2£©=0£¬¹Źx=+1”£¹ŹŃ”A”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”2018½ģ¾ÅÄź¼¶ĻĀѧʌæŖŃ§æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗ×ŪŗĻĢā
£Ø1£©³õÖŠ»ÆѧӊŠķ¶ąŹµŃ飬Čō°“ÕÕŹµŃéÖ÷ŅŖÄæµÄæɽ«ŹµŃé·ÖĪŖ£ŗĢ½¾æ»Æѧ·“Ó¦Ē°ŗóĪļÖŹµÄÖŹĮæ¹ŲĻµ”¢Ģ½¾æĪļÖŹµÄĪļĄķ»ņ»ÆѧŠŌÖŹ”¢Ģ½¾æĪļÖŹµÄŗ¬Į攢Ģ½¾æ»Æѧ·“Ó¦Ģõ¼žµČ£¬¾Ż“ĖÓ¦½«ĻĀĮŠŹµŃéÖŠµÄCÓė____£ØĢī”°A”±»ņ”°B”±»ņ”°C”±»ņ”°D”±£©¹éĪŖŅ»Ąą£¬ŅĄ¾ŻŹĒ_____”£
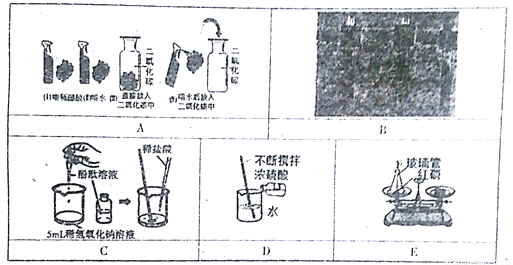
£Ø2£©æĪĶāѧĻ°ÖŠ·¢ĻÖ£¬Ķس£ĒéæöĻĀ£¬Č¼ÉÕŹĒÖøæÉČ¼ĪļŌŚŃõĘųÖŠ·¢¹ā·ÅČČµÄ¾ēĮŅµÄŃõ»Æ·“Ó¦£¬ĄżČē£ŗCH4+2O2µćČ¼ CO2+2H2O£¬ŃõĘųŹĒ“Ė·“Ó¦µÄŃõ»Æ¼Į£¬Č»¶ųČ¼ÉÕ²»Ņ»¶ØŠčŅŖŃõĘų£¬ŌŚ¹āÕÕĢõ¼žĻĀ£¬¼×ĶéŌŚĀČĘųÖŠŅ²ÄÜČ¼ÉÕ£¬ĒŅ²śĪļÓė¼×ĶéŌŚŃõĘųÖŠ³ä·ÖČ¼ÉյIJśĪļĻąĖĘ£¬ĒėŠ“³ö¼×ĶéŌŚ×ćĮæĀČĘųÖŠ³ä·ÖČ¼ÉյĻÆѧ·½³ĢŹ½£ŗ______£¬“Ė·“Ó¦ÖŠµÄŃõ»Æ¼ĮŹĒ_____”£
A,D, ¶¼Ģ½¾æĪļÖŹµÄĪļĄķ»ņ»ÆѧŠŌÖŹ CH4+4Cl2CCl4+4HCl, Cl2 ”¾½āĪö”æ£Ø1£©¾Ż“ĖÓ¦½«ĻĀĮŠŹµŃéÖŠµÄCÓėA”¢D¹éĪŖŅ»Ąą£¬ŅĄ¾ŻŹĒ£ŗ¶¼Ģ½¾æĪļÖŹµÄĪļĄķ»ņ»ÆѧŠŌÖŹ£»£Ø2£©ŌŚ¹āÕÕĢõ¼žĻĀ£¬¼×ĶéŌŚĀČĘųÖŠŅ²ÄÜČ¼ÉÕ£¬ĒŅ²śĪļÓė¼×ĶéŌŚŃõĘųÖŠ³ä·ÖČ¼ÉյIJśĪļĻąĖĘ£¬Ōņ¼×ĶéŌŚ×ćĮæĀČĘųÖŠ³ä·ÖČ¼ÉÕÉś³ÉĖÄĀČ»ÆĢ¼ŗĶĀČ»ÆĒāĘųĢ壬»Æѧ·½³ĢŹ½ĪŖ£ŗCH4+4Cl2CCl4+4HCl£¬“Ė·“Ó¦ÖŠµÄŃõ»Æ¼ĮŹĒCl2”£ ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”2018½ģ¾ÅÄź¼¶ĻĀѧʌæŖŃ§æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¹Ųӌ׏Ō“”¢ÄÜŌ“”¢»·±£·½ĆęµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
A. æÕĘųÖŠŗ¬Įæ×ī¶ąµÄ»ÆŗĻĪļĪŖ¶žŃõ»ÆĢ¼
B. µŲĒņÉĻµÄŗ£Ė®¶ą£¬Ā½µŲÉĻµÄĖ®Č“ŗÜÉŁ£¬Ā½µŲÉĻµÄĖ®Ö»Ō¼Õ¼Č«ĒņĖ®“¢ĮæµÄ3.5%
C. īŃŗĶīŃŗĻ½š¾ßÓŠĆܶȊ””¢ČŪµćµĶ”¢æÉĖÜŠŌŗĆ”¢Ņ×¼Ó¹¤µČÓÅĮ¼ŠŌÄÜ
D. æÉČ¼±ł½«µŲ³ÉĪŖĪ“Ą“ÖŲŅŖµÄŠĀÄÜŌ“
C ”¾½āĪö”æA”¢æÕĘųÖŠŗ¬Įæ×ī¶ąµÄ»ÆŗĻĪļĪŖ¶žŃõ»ÆĢ¼£¬ÕżČ·£»B”¢µŲĒņÉĻµÄŗ£Ė®¶ą£¬Ā½µŲÉĻµÄĖ®Č“ŗÜÉŁ£¬Ā½µŲÉĻµÄĖ®Ö»Ō¼Õ¼Č«ĒņĖ®“¢ĮæµÄ3.5%£¬ÕżČ·£»C”¢īŃŗĶīŃŗĻ½š¾ßÓŠŗܶąÓÅĮ¼µÄŠŌÄÜ£¬ČēČŪµćøߣ¬ĆܶȊ”£¬æÉĖÜŠŌŗĆ£¬Ņ×ÓŚ¼Ó¹¤£¬»śŠµŠŌÄÜĒæµČ£¬ÓČĘäŹĒīŃŗĶīŃŗĻ½šµÄæ¹øÆŹ“ŠŌÄÜ·Ē³£ŗĆ£¬“ķĪó£»D”¢æÉČ¼±ł½«µŲ³ÉĪŖĪ“Ą“ÖŲŅŖµÄŠĀÄÜŌ“£¬ÕżČ·”£¹ŹŃ”C”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗŗŚĮś½Ź”2018½ģ¾ÅÄź¼¶ĻĀѧʌæŖŃ§æ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠŹµŃ黳±¾²Ł×÷“ķĪóµÄŹĒ£Ø £©
A.  ŅŗĢåµÄĒćµ¹ B.
ŅŗĢåµÄĒćµ¹ B.  ¼ģŃéŃõĘųŹĒ·ń¼ÆĀś C.
¼ģŃéŃõĘųŹĒ·ń¼ÆĀś C.  øųŅŗĢå¼ÓČČ D.
øųŅŗĢå¼ÓČČ D.  ³ĘČ”Ņ»¶ØÖŹĮæµÄNaOH
³ĘČ”Ņ»¶ØÖŹĮæµÄNaOH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”ŃĪ³ĒŹŠ±õŗ£ĻŲµŚĖĽĢÓż¼ÆĶÅ2018Äź“ŗѧʌ»ÆѧŌĀæ¼Ä£ÄāŹŌ¾ķ ĢāŠĶ£ŗµ„Ń”Ģā
æÕĘųÖŠŗ¬Įæ×ī¶ą£¬ĒŅæÉŅŌ×ö±£»¤ĘųµÄĘųĢåŹĒ
A. ŃõĘų B. µŖĘų C. ¶žŃõ»ÆĢ¼ D. Ļ”ÓŠĘųĢå
B ”¾½āĪö”æA£®ŃõĘųŹĒŅ»ÖÖ»ÆѧŠŌÖŹ±Č½Ļ»īĘƵÄĘųĢ壬ÄÜŗĶŠķ¶ąĪļÖŹ·¢Éś·“Ó¦£¬²»ÄÜÓĆ×ö±£»¤Ęų£»¹ŹA“ķĪó£»B£®æÕĘųµÄ³É·Ö°“Ģå»ż·ÖŹż¼ĘĖć“óŌ¼ŹĒ£ŗ“óŌ¼ŹĒµŖĘųÕ¼(78%)£¬ŃõĘųÕ¼(21%)£¬Ļ”ÓŠĘųĢåÕ¼(0.94%)£¬¶žŃõ»ÆĢ¼Õ¼(0.03%)£¬ĘäĖüĘųĢåŗĶŌÓÖŹÕ¼(0.03%)£¬ĘäÖŠ×ī¶ąµÄŹĒµŖĘų£¬ÓÉÓŚµŖĘųµÄ»ÆѧŠŌÖŹ²»»īĘĆ£¬ĖłŅŌæÉÓĆ×ö±£»¤Ęų£»¹ŹBÕżČ·£»C£®¶žŃõ»ÆĢ¼ŌŚæÕĘųÖŠÕ¼µÄĢå»ż·ÖŹżĪŖ£ŗ0.03%£¬²»ŹĒŗ¬Įæ×ī¶ąµÄ...²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”¾ø½ŹŠ2018½ģ¾ÅÄź¼¶ĻĀѧʌµŚŅ»“Ī¶ĄĮ¢×÷Ņµ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
A”«GĪŖ³õÖŠ»Æѧ³£¼ūĪļÖŹ,Ļą»„¹ŲĻµČēĶ¼ĖłŹ¾£¬”°”ś”±±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬”°”Ŗ”±±ķŹ¾Ļą»„Ö®¼äÄÜ·¢Éś·“Ó¦£Ø²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žŹ”ĀŌ£©”£ĘäÖŠA”¢FŹĒĮ½ÖÖ³£¼ūµÄŃõ»ÆĪļ£»B”¢DŹĒĮ½ÖÖ³£¼ūµÄ¼ī£» GæÉÓĆ×÷½ØÖž²ÄĮĻ£»C³£ÓĆÓŚĻ“µÓ¼ĮµÄÉś²ś£»A”¢B”¢C”¢EĖłŹōĪļÖŹĄą±š²»Ķ¬”£Ēė»Ų“šĻĀĮŠĪŹĢā”£

£Ø1£©AµÄ»ÆѧŹ½___________£¬GµÄ»ÆѧŹ½__________”£
£Ø2£©DµÄÓĆĶ¾ÓŠ__________£ØŠ“³öŅ»ÖÖ¼“æÉ£©”£
£Ø3£©Š“³ö»Æѧ·“Ó¦¢Ł¢Ś¢ŪµÄ»Æѧ·½³ĢŹ½£ŗ
¢Ł__________£»
¢Ś__________£»øĆ·“Ó¦ŹōÓŚĖÄÖÖ»ł±¾·“Ó¦ĄąŠĶÖŠµÄ__________·“Ó¦”£
¢Ū__________”£
CO2 CaCO3£ØĆū³Ę²»øų·Ö£© øÄĮ¼ĖįŠŌĶĮČĄ»ņÅäÖĘÅ©Ņ©²Ø¶ū¶ąŅŗ»ņ×÷½ØÖž²ÄĮĻµČ£ØŗĻĄķ¼“æÉ£© CaO + H2O =Ca(OH)2 Na2CO3+ Ca(OH)2=CaCO3”ż+2NaOH ø“·Ö½ā CO£² + 2NaOH =Na2CO3+ H2O ”¾½āĪö”æAŹĒŃõ»ÆĪļ£¬B”¢DŹĒ¼ī£¬øł¾Ż¼īµÄŠŌÖŹæÉÖŖ¼īÄÜÓė·Ē½šŹōŃõ»ÆĪļ·“Ó¦£¬¹ŹAæÉÄÜŹĒ¶žŃõ»ÆĢ¼£»GæÉÓĆ×÷½ØÖž²ÄĮĻ£¬ÄĒĆ“GŹĒĢ¼ĖįøĘ£»C³£ÓĆÓŚĻ“µÓ¼ĮµÄÉś²ś£¬...²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com