


分析 (1)石灰石的主要成分为碳酸钙,可以和稀盐酸反应生成氯化钙、水和二氧化碳,可以据此写出该反应的化学方程式;碳酸氢钠在加热的条件下分解产生二氧化碳,所应该选择固固加热型的反应装置;
(2)通入的二氧化碳不可能被全部反应掉,为了得到较纯净的氧气,应该在③中加入氢氧化钠溶液来吸收二氧化碳,可以据此解答;
(3)氧气难溶于水且密度比空气大,所以可以选择排水法或是向上排空气法来收集,可以据此选择装置.
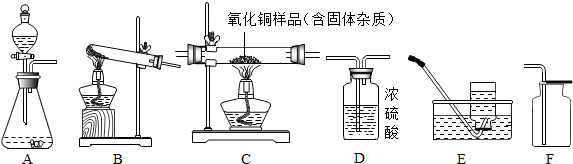
解答 解:(1)石灰石的主要成分为碳酸钙,可以和稀盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;碳酸氢钠在加热的条件下分解产生二氧化碳,所应该选择固固加热型的反应装置即A装置;
(2)通入的二氧化碳不可能被全部反应掉,为了得到较纯净的氧气,应该在③中加入氢氧化钠溶液来吸收二氧化碳;
(3)氧气难溶于水且密度比空气大,所以可以选择排水法或是向上排空气法来收集,即C或E装置.
故答案为:(1)CaCO3+2HCl═CaCl2+CO2↑+H2O;A;
(2)NaOH溶液;除去二氧化碳;
(3)C、E.
点评 本题考查了过氧化钠与二氧化碳的反应及其反应产物氧气和气体的除杂,完成此题,可以依据题干提供的信息以及已有的知识进行.


科目:初中化学 来源: 题型:多选题
| 选项 | 实验目的 | |
| A | 证明MnO2能够改变过氧化氢的分解速率 | 在两只试管中分别取5mL、10%的过氧化氢溶液,一个试管中加入少量MnO2,并分别用带火星的木条检验 |
| B | 除去氯化镁固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 检验二氧化碳气体中含有少量的一氧化碳 | 通过过量灼热的氧化铜 |
| D | 分离碳酸钠和氢氧化钠的混合物 | 加入过量氢氧化钙溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 | |
| C. | 青蒿素不属于有机化合物 | |
| D. | 青蒿素中氢元素的质量分数为7.8% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 营养成分:每100克产品中 | |
| 能量≥236千焦 | 蛋白质≥2.8克 |
| 脂肪≥2.9克 | 糖类≥3.4克 |
| 铁≥56毫克 | 钙≥93毫克 |
| A. | 不含油脂 | B. | 可补充钙元素和铁元素 | ||
| C. | 含有维生素C | D. | 100g该酸牛奶中可能含有3g糖 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的稀硫酸的质量/g | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体的质量/g | 4.2 | 3.4 | 3.0 | 3.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com