
分析 (1)乙醇充分燃烧生成二氧化碳和水,可以根据化学方程式和乙醇的质量计算二氧化碳的质量.当然也可以根据碳元素守恒直接求算二氧化碳的质量.
(2)由于不充分燃烧,同时也没给出对应的化学方程式,所以要根据碳元素守恒直接求算一氧化碳对应的碳元素的质量,进而求算出一氧化碳的质量.
解答 解:
(1)设69g乙醇充分燃烧生成的二氧化碳的质量为x.
C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O
46 88
69g x
$\frac{46}{88}$=$\frac{69g}{x}$
x=132g.
答:生成二氧化碳的质量为132g
(2)69g乙醇中碳元素的质量为69g×$\frac{12×2}{12×2+1×6+16}$×100%=36g
生成的二氧化碳中碳元素的质量为88g×$\frac{12}{12+16×2}$×100%=24g
则一氧化碳对应的碳元素的质量为36g-24g=12g
则对应的一氧化碳的质量为12g÷($\frac{12}{12+16}$×100%)=28g
答:生成的一氧化碳的质量为28g.
点评 乙醇不充分燃烧时要根据碳元素和氢元素进行相关的分析和计算,而不是去硬性套化学方程式,或者是凑不充分燃烧的化学方程式.


科目:初中化学 来源: 题型:选择题
| A. | 该“塑化剂”属有机物 | |
| B. | 该“塑化剂”中碳、氢、氧三种元素的质量比为12:17:2 | |
| C. | 该“塑化剂”属氧化物 | |
| D. | 该“塑化剂”由24个碳原子、34个氢原子、4个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
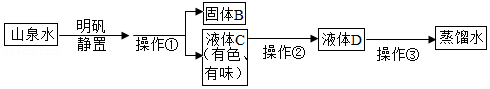
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
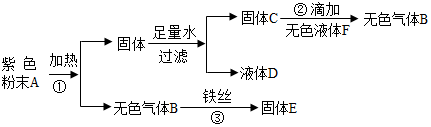
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:
A、B、C、D、E、F分别是氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液、一氧化碳、二氧化碳中的一种.他们之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应,固态C物质可用于人工降雨.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com