阜宁县实验初中某化学研究性学习小组为了探究水垢的成因和主要成分,从教材和互联网上查得如下资料:
(Ⅰ)锅炉用水硬度高了十分危险,因为锅炉内结垢后不仅浪费燃料,而且会使锅炉内管道局部过热,易引起管道变形或损坏,严重时还可能引起爆炸.(上册第56页)
(Ⅱ)用适量的盐酸可以将热水瓶胆壁上的水垢[主要成分是Mg(OH)2和CaCO3]除去.(下册第65页)
(Ⅲ)天然水中一般都含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢.
1李同学对该井水进行如下探究,其做法及结论合理的是______.(填序号)
(A)用烧杯取少量该井水,加入适量肥皂水,搅拌,发现有较多浮渣产生,说明该井水为硬水.
(B)用烧杯取少量井水,加入一定量活性炭,搅拌、过滤,可吸附井水中的钙、镁离子,并使井水软化.
(C)取较多井水,加热煮沸,煮沸后的井水硬度降低.
(2)某同学为了粗略测定某锅炉水垢中CaCO3的质量分数,取6.0g 样品,逐滴加入稀盐酸至不再产生气泡为止,共生成2.2gCO2 气体.试计算样品中CaCO3的质量分数.
解:(1)A、区分硬水和软水可加肥皂水,产生泡沫少的是硬水,正确;B、活性炭只能吸附色素和异味,不能吸附钙镁离子,不能将硬水变成软水,B错误;C、加热煮沸,水中的钙镁离子化合物能转化成沉淀,从而降低硬度,正确,故选AC
(2)设6.0g锅炉水垢样品中CaCO
3的质量为x
CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑
100 44
x 2.2g
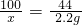
x=5.0g
锅炉水垢样品中碳酸钙的质量分数=
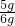
×100%=83.3%
答:锅炉水垢样品中碳酸钙的质量分数为83.3%.
故答案为:(1)AC
(2)83.3%
分析:(1)根据硬水软水的区分方法及硬水软化的方法分析
(2)根据反应的化学方程式,由生成二氧化碳的质量计算样品中碳酸钙的质量,求得样品中碳酸钙的质量分数;
点评:本题考查硬水软水的鉴别及硬水软化方法以及根据化学方程式的计算,注重基础.

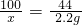
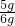 ×100%=83.3%
×100%=83.3%
