
【题目】溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。

(1)t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是____。
(2)某同学按图所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是___(填字母)。
(3)t3℃时要把150g甲物质的饱和溶液中稀释成质量分数为20%的溶液,需加入水的质量为____克。
【答案】丙>乙>甲 B 100
【解析】
(1)由溶解度曲线可知,在t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是:丙>乙>甲;
②由图可知,t1℃时甲的溶解度大于14g,故A是不饱和溶液;t2℃时甲物质的溶解度是28g,即100g水中最多可以溶解28g甲物质,所以B溶液是饱和溶液;t3℃时甲物质的溶解度是50g,在C溶液中含有溶质的质量是42g,是不饱和溶液;故填B。
③t3℃时,甲物质的溶解度是50g, 故150g饱和溶液中溶质的质量分数为:![]() ×100%=33.3% ,设把150g甲物质的饱和溶液中稀释成质量分数为20%的溶液,需加入水的质量为x,150g×
×100%=33.3% ,设把150g甲物质的饱和溶液中稀释成质量分数为20%的溶液,需加入水的质量为x,150g×![]() ×100%=(150g+x)×20%,解得x=100g
×100%=(150g+x)×20%,解得x=100g


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:
【题目】请用化学用语填空:
(1)三个氯原子:_____;
(2)保持二氧化硫的化学性质的最小粒子_____;
(3) 2个镁离子_____;
(4)五氧化二磷中磷元素的化合价_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室配制50克质量分数为12%的氯化钠溶液。下图是小军实验操作过程示意图:
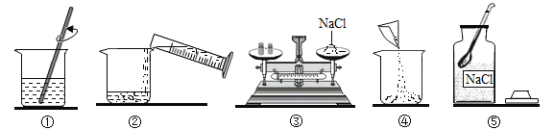
(1)请指出图中一处明显错误的操作_________;改正操作后,用上述图示的序号表示配制溶液的正确操作顺序________;
(2)图①中玻璃棒搅拌的目的是_______;
(3)配制该溶液需要用_________的量筒(填“50mL”、“100mL”或“200mL”)量取水。用己调节平衡的天平称取氯化钠固体时,发现指针偏右,接下来的操作是_______;
(4)经检验,该同学配制的溶液溶质质量分数偏小,可能的原因是_____ ( 填序号)
A 氯化钠固体不纯
B 用生锈的砝码称量
C 装瓶时有少量液体洒出
D 用量筒量取水时,俯视读数
E 溶解的烧杯提前用蒸馏水润洗
(5)将20克12%的氯化钠溶液配制成6%的氯化钠溶液,需加水______克。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】资料显示:在一定温度下,往煤中加入适量石灰石粉,其分解产物可使煤(含S)燃烧时产生的SO2转化成CaSO4,从而减少SO2排放,该方法被称为钙基固硫。某实验小组利用下列实验装置和药品对其可行性进行了模拟探究。
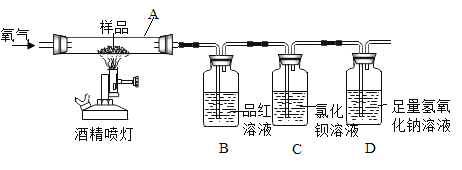
①SO2与CO2为非金属氧化物,均能与碱溶液反应,但SO2有毒,能与品红作用使其褪色。
②2SO2+2H2O+O2+2BaCl2=2BaSO4↓+4HCl
③CO2不与BaCl2溶液反应
(实验一)取S粉与CaCO3粉末的混合物装入A中,连续通入过量O2,加热至500℃左右,充分反应后,发现B中红色消失、C中出现大量的白色浑浊。
(1)停止实验的正确操作是_____。
(2)装置D中NaOH的作用是_____。
(实验二)另取上述S粉与CaCO3粉末的混合物装入A中,连续通入过量O2,并迅速加热升温,控制在1000℃左右,充分反应后,发现B中红色消失,C中出现少量的白色浑浊。
(3)取反应后D中溶液滴加过量盐酸,出现大量无色气泡(其中有CO2)。反应结束后,经实验检验A中余下固体含有CaSO4,由此得知实验二过程中,A中发生的反应有三个,请完成剩余的两个化学方程式:
①S+O2![]() SO2;
SO2;
②_____;
③_____。
(实验三)另取CaSO4粉末装入A中,连续通入过量O2,加热至1200℃左右,充分反应,发现B中红色消失。
(4)比较实验一、二、三可知,如用该方法固硫,适宜的温度条件是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“分子运动现象”是自然界的普遍现象。图1是27 ℃时氢分子和氧分子运动的微观示意图;图2是“探究分子运动现象"的实验。

(1)图1说明:温度相同时,气体分子的质量越大,分子运动越_____(填“快”或 “慢”)。
(2)已知浓氨水挥发出的氨气与浓盐酸挥发出的氯化氢气体相遇时会产生白烟,该变化属于_____(填“物理变化"或“化学变化”)。图2中A、B、C三处最先产生白烟的是_____处。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年为“元素周期表年”,元素周期表是学习和研究化学的重要工具。原子序数为1-18的元素在元素周期表中的部分信息如图所示。请回答下列问题:

(1)一个磷原子的质子数为_____。
(2)铝属于_____(填“金属”或“非金属”)元素,在化学反应中容易_____(填“得”或“失”)电子,形成的铝离子的化学符号为_____。
(3)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的_____相同。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某粒子的结构示意图,下列说法正确的是
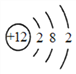
A. 该粒子有12个质子
B. 该粒子有2个电子层
C. 该粒子属于非金属元素
D. 该粒子已达到相对稳定结构
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】九年级课外活动小组的同学们在期末复习时,来到化学实验室亲自对“质量守恒定律”进行了再次探究,如图是他们根据这一学期学过的化学反应分别设计的实验,请你一起参与他们的探究活动,并回答相关问题
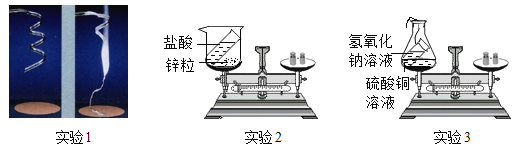
实验1:称量镁条,点燃,待反应结束后,再称量。
实验2:将盛有稀盐酸的小试管放入盛有锌粒的烧杯中称量,然后使稀盐酸与锌粒接触,充分反应后再称量实验3:将盛有氢氧化钠溶液的小试管放入盛有硫酸铜溶液的锥形瓶中称量,然后使氢氧化钠溶液与硫酸铜溶液混合,充分反应后再称量。
编号 | 实验1 | 实验2 | 实验3 |
反应前称重质量 | 9.6g | 212.6g | 118.4g |
反应后称重质量 | 16.0g | 212.4g | 118.4g |
(1)实验1观察到的现象是_______________;
(2)写出实验3反应的化学方程式________________;
(3)上述三个反应______________(填“符合”或“不符合”)质量守恒定律,实验___________正确反映了反应物与生成物的质量关系;
(4)由上述实验我们得到启示,探究_______________的反应验证质量守恒定律,实验必须在密闭的装置中进行;
(5)由质量守恒定律可知,化学反应前后,一定不变的是 _____________(填序号);
①物质种类 ②元素种类 ③原子种类 ④分子种类 ⑤分子数目 ⑥原子数目
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应):
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 4.24 | 4.16 | 4.08 | 4.08 |
试计算:
(1)完全反应后产生的氧气的总质量为_______。
(2)样品中氯酸钾的纯度是多少_______?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com