
【题目】小周在适宜的条件下,利用 KNO3 晶体和溶质质量分数为 20%的 KNO3 溶液,配制一定溶质质量分数的 KNO3 溶液。取 40克 KNO3 晶体置于烧杯中,并依次加入溶质质量分数为 20%的KNO3 溶液并充分搅拌溶解,其过程如图所示:

(1)在配制过程各阶段的溶液中属于饱和溶液的有_____。(填烧杯序号)
(2)计算④号烧杯中溶液的溶质质量分数(结果精确到0.1%)____________。
(3)已知KNO3晶体的溶解度随温度的升高而增大,在不考虑水分蒸发的情况下,在配制过程中,下列操作会导致④号烧杯中溶液的溶质质量分数偏大的有_____。
A 所用 KNO3 晶体混有少量泥沙 B 配制过程中环境温度升高
C 用砝码生锈的天平称取 40克K NO3 晶体 D 溶解时没有用玻璃棒搅拌
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_____产生,反应的化学方程式是_____。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
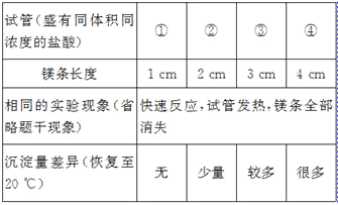
[得出结论]镁条与盐酸反应产生白色沉淀与_____有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是_____(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | _____,白色沉淀_____ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀_____ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、_____ |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动。
探究1:研究常见的物质——氢氧化钠和盐酸的反应程度。
实验内容 | 实验现象 | 解释与结论 |
取反应后少量溶液于试管中,加入固体化合物___________。 | _________ | 盐酸过量 |
探究2:研究酸的性质——硫酸、盐酸和锌反应
通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气。产生这种共同现象的原因为________________________________________________________________________。
探究3:探索未知——浓硝酸和铜制取气体。
已知![]() 。NO2能和水反应生成硝酸和NO。NO和NO2都是空气的污染物。
。NO2能和水反应生成硝酸和NO。NO和NO2都是空气的污染物。
(1)利用该反应制取二氧化氮的发生装置,应选用图所示装置中的________。收集NO2的方法为________。
(2)反应NO+X→NO2中,X的化学式应为________;若用浓硝酸和铜制取NO,应采用的收集方法是________________________________________________________________________。
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,那么所加碳酸钠溶液的溶质质量分数为________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.
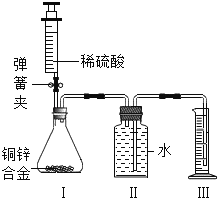
探究过程如下:
①连接实验装置并检查装置气密性.
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL.(注:样品中的杂质不参加反应)
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量1.4g.
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数.
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09g/L.
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为 ,实验过程中须加入稀硫酸至不再产生气体,目的是 .
(2)步骤③中称量剩余固体之前的正确操作是 、洗涤、干燥.
(3)根据实验测定的数据,上述三位同学中 (填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数.
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差.以下因素可能造成偏差的有 (填标号).
A.移出装置Ⅲ时,导管内留存了一部分水
B.实验测量前,没有排除装置Ⅰ中的空气
C.数据处理时,未排除加入稀硫酸所占的体积.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用以下装置探究碳及其氧化物的某些性质。

(1)写出仪器①的名称_____。
(2)写出 A 中反应的化学方程式_____。
(3)C 装置利用了浓硫酸的_____性。
(4)D 装置中玻璃管内反应的化学方程式为_____。
(5)F 装置除了吸收 CO2 外,还可以起到的作用是_____。
(6)在实验过程中,一氧化碳和氧化铜反应不仅能生成铜,还可能生成少量氧化亚铜(化 学式为 Cu2O)。如果实验前在 E 中放入氧化铜的质量为 2.0g,氧化铜全部反应完后,E 中固体质量可能为_____(填字母)。
A 1.55g B 1.60g C 1.65g D 1.82g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_____产生,反应的化学方程式是_____。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
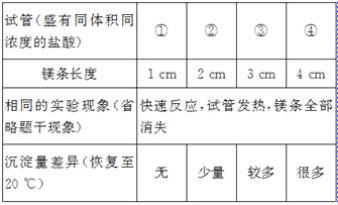
[得出结论]镁条与盐酸反应产生白色沉淀与_____有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是_____(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | _____,白色沉淀_____ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀_____ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、_____ |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com