
下列课外实验与物质的化学性质无关的是
A. 用石墨做导电实验
B. 用灼烧法区分棉纤维与羊毛纤维
C. 用白糖、小苏打、柠檬酸等自制汽水
D. 用紫甘蓝的酒精浸取液检验苹果汁与石灰水的酸碱性
A 【解析】物理性质是指物质不需要经过化学变化就直接表现出来的性质。化学性质是指物质经过化学变化表现出来的性质。A、用石墨做导电实验,导电性属于物理性质;B、用灼烧法区分棉纤维与羊毛纤维,羊毛纤维有烧焦的羽毛气味,属于化学性质;C、用白糖、小苏打、柠檬酸等自制汽水,小苏打呈碱性,柠檬酸呈酸性,均属于化学性质;D、用紫甘蓝的酒精浸取液检验苹果汁与石灰水的酸碱性,甘蓝的酒精浸取液制成酸碱指示剂,...科目:初中化学 来源:广东省广州市海珠区2018年九年级中考一模化学试卷 题型:单选题
下列说法中,正确的是
A. 浓硫酸需要密封保存的原原因是防止其挥发
B. 酸碱中和反应,必须加入指示剂才能判断中和反应的发生
C. 用稀盐酸能把镁粉、氧化铜粉和木炭粉区别开
D. 在pH为3的某溶液中加入pH为5的另一种溶液,可使溶液的pH提高到8
C 【解析】A、浓硫酸需要密封保存,是因为具有吸水性,而不是挥发,错误;B、酸碱中和反应中有的不需要加入指示剂,例如氢氧化铜与硫酸反应,氢氧化铜固体会逐渐消失,错误;C、镁粉能与稀盐酸反应生成氢气,氧化铜能与稀盐酸反应生成氯化铜和水,会观察到黑色粉末逐渐溶解,溶液变蓝,木炭粉不与稀盐酸反应,可以鉴别,正确;D、pH为3的某溶液中加入pH为5的另一种溶液,其pH会在3~5之间,不能使溶液的pH...查看答案和解析>>
科目:初中化学 来源:湖北省黄石市2018届九年级5月份联考化学试卷 题型:科学探究题
某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.
(提出问题)剩余固体成分是什么?
(提出猜想)猜想Ⅰ.全部是碳酸钙
猜想Ⅱ. _________ 猜想Ⅲ.既有碳酸钙,也有氧化钙
(设计并完成实验)
实验操作 | 实验现象 | 实验结论 |
(1)取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有_____。 |
(2)再取少量固体于另一试管中滴加过量___。 | 有气泡生成 | 说明猜想Ⅲ正确. |
(交流与分析)取操作(1)中的清液于另一支试管中通入CO2,发生的反应是_____(用化学方程式表)。
若剩余固体的成分与猜想Ⅰ相符,则可能的原因是_________(答一条)
全是氧化钙 氧化钙 稀盐酸 CO2 + Ca(OH)2== CaCO3↓+ H2O 加热时间过短(或没达到碳酸钙的分解温度,合理即可) 【解析】【提出猜想】猜想Ⅱ.碳酸钙高温分解生成氧化钙和二氧化碳,碳酸钙可能全部分解,所以猜想全是氧化钙。【设计并完成实验】(1)酚酞遇碱性溶液变红,取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液,溶液变红,说明固体成分中一定含有氧化钙,因为Ca...查看答案和解析>>
科目:初中化学 来源:广东省2018届九年级下学期第二次月考化学试卷 题型:简答题
某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液,他们的实验过程和相关数据如图所示。请计算:
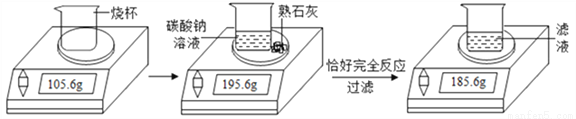
(1)实验中生成沉淀的质量为________g;
(2)所得氢氧化钠溶液中溶质的质量分数为___________。
10 10% 【解析】试题分析:利用化学方程式,根据反应的质量比即可计算出个物质的质量。 设氢氧化钠的质量为x; Ca(OH)2 + Na2CO3 ="=" CaCO3↓ + 2NaOH 100 80 10g x 100/80 =10g/x X=8g 所的溶液的质量=185.6g-105.6g=80g 氢氧化钠溶液的溶质质量分数=8g/80g ...查看答案和解析>>
科目:初中化学 来源:广东省2018届九年级下学期第二次月考化学试卷 题型:单选题
下列验证Zn、Fe、Ag三种金属活动性顺序的实验方案中(“-”表示未进行金属与盐溶液之间的实验),不能达到实验目的是

A. A B. B C. C D. D
C 【解析】试题分析:根据金属活动性顺序的应用,位于前面的金属能把位于后面的金属从化合物的溶液中置换出来。故要判断Zn、Fe、Ag三种金属活动性顺序的应用最简单的方法是取中间的金属和两边金属的溶液或取两边的金属和中间金属的溶液。C中不能判断出铁和银的活动性顺序,故选C。查看答案和解析>>
科目:初中化学 来源:云南省2018届初三统一考试化学试卷 题型:流程题
粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如下图所示:
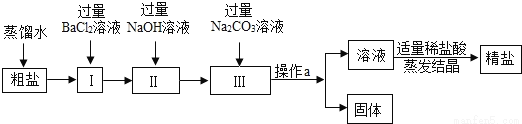
(1)操作a的名称是__________,该操作需要用到的玻璃仪器主要有:烧杯、_________、玻璃棒;
(2)写出I中发生反应的化学方程式_____________________;
(3)加入过量Na2CO3的作用是_________________________。
过滤, 漏斗; BaCl2+ Na2SO4 = BaSO4↓+ 2NaCl ; 除尽溶液中的CaCl2 和过量的BaCl2 (符合题意即可); 【解析】(1) 操作a的名称是过滤,通过过滤能够把液体和固体分离,该操作需要用到的玻璃仪器主要有:烧杯、漏斗、玻璃棒;(2) I中氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,发生反应的化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl;(...查看答案和解析>>
科目:初中化学 来源:云南省2018届初三统一考试化学试卷 题型:单选题
有甲、乙、丙、丁四种金属。只有甲在自然界主要以游离态存在。丁盐的水溶液不能用乙制的容器盛放,但可以用丙制的容器盛放。这四种金属的活动性由强到弱的顺序是
A. 甲>乙>丁>丙 B. 丙>丁>乙>甲
C. 丙>乙>丁>甲 D. 乙>丁>丙>甲
D 【解析】只有甲在自然界主要以单质形式存在,说明甲的活动性最弱,丁盐的水溶液不能用乙制的容器盛放,但可用丙制的容器盛放,说明乙比丁活泼,丁比丙活泼,故活动性顺序为:乙>丁>丙>甲,故选D。查看答案和解析>>
科目:初中化学 来源:2018年5月23日 化学式和化合价--《每日一题》2017-2018学年九年级化学人教(下) 题型:单选题
硼氢化钠(NaBH4,其中氢元素的化合价为﹣1)是一种安全车载氢源。有关硼氢化钠的说法正确的是
A. 硼元素的化合价为+3
B. 只含一种非金属元素
C. Na、B、H三种元素的质量比为1∶1∶4
D. 含2个氢分子
B 【解析】A.钠元素显+1价,氢元素的化合价为﹣1,设硼元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣1)×4=0,则x=+3价,故选项说法正确.B.硼氢化钠(NaBH4)中,硼元素与氢元素均为非金属元素,故选项说法错误.C.Na、B、H的质量比为(23×1):(11×1):(1×4)≠1:1:4,故选项说法错误.D.硼氢化钠是由硼氢化钠分子构成的,不含氢分...查看答案和解析>>
科目:初中化学 来源:江苏省扬州市宝应县2018届九年级下学期中考二模考试化学试卷 题型:科学探究题
某研究小组为探究“铁钉在不同溶液中腐蚀的速率”,在相同条件下取同浓度的下列不同溶液用如图装置完成实验,并用手持数据采集器进行测定。回答下列问题:

(1)铁锈的主要成分的化学式为____________
(2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的酸性均变____________(填“强”或“弱”)
(3)上述实验方案是否合理?_________(填“合理”或“不合理”),你的理由是__________
(4) 该小组在不同酸碱性溶液中又进行了探究,在相同条件下其测定的实验数据如下图:

①上述实验中,氧气浓度下降先陡后缓的原因为________________
②根据甲、乙图像,可看出:铁钉在酸性溶液中比在中性溶液中生锈________(填“快”或“慢”, 下同);在开始时PH相同的情况下,甲、乙组中均为含氯离子的溶液生锈________ 。
Fe2O3 弱 不合理; 实验前溶液的PH没有保持相同 氧气浓度下降使腐蚀速率变慢。 快 快 【解析】本题主要考查了影响化学反应速率的因素探究,铁锈蚀的原理,溶液的酸碱性与pH值的关系。 (1)铁锈的主要成分是氧化铁,化学式为Fe2O3; (2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的pH都在增大,酸性均变弱; (3)上述实验方案不合...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com