写出以下化学反应的方程式并注明反应(1)、(2)的基本类型
(1)镁条在空气中燃烧______(______).
(2)氯酸钾与二氧化锰混合加热制氧气______(______).
(3)二氧化碳通入紫色石蕊试液中______.
(4)硝酸银见光分解生成一种金属、一种红棕色气体(NO2)和一种能支持燃烧的气体______.
解:(1)镁条在空气中燃烧生成了氧化镁,反应的方程式是:2Mg+O
2
2MgO,该反应由两种物质生成了一种物质,属于化合反应;
(2)氯酸钾在二氧化锰的催化作用下生了氯化钾和氧气,反应的方程式是:2KClO
3 
2KCl+3O
2↑,该反应由一种物质生成了两种物质,属于分解反应;
(3)二氧化碳通入紫色石蕊试液中,二氧化碳与水反应生成了碳酸,能使紫色石蕊试液变红,反应的方程式是:CO
2+H
2O=H
2CO
3;
(4)硝酸银见光分解生成一种金属、一种红棕色气体(NO
2)和一种能支持燃烧的气体,根据质量守恒定律可知,这种金属应是银,能支持燃烧的气体是氧气,反应的方程式是:2AgNO
3
2Ag+2NO
2↑+O
2↑.
故答为:(1)2Mg+O
2
2MgO,属于化合反应;(2)2KClO
3 
2KCl+3O
2↑,分解反应;
(3)CO
2+H
2O=H
2CO
3;(4)2AgNO
3
2Ag+2NO
2↑+O
2↑.
分析:根据给出的反应分析反应物、生成物及反应条件,再根据书写化学方程式的步骤和要求写出方程式;根据反应物、生成物的种类及反应的特点判断反应的基本类型.
点评:本题主要考查了书写化学方程式的方法和步骤,会根据反应物、生成物、反应条件,正确书写化学方程式.

 2MgO,该反应由两种物质生成了一种物质,属于化合反应;
2MgO,该反应由两种物质生成了一种物质,属于化合反应; 2KCl+3O2↑,该反应由一种物质生成了两种物质,属于分解反应;
2KCl+3O2↑,该反应由一种物质生成了两种物质,属于分解反应; 2Ag+2NO2↑+O2↑.
2Ag+2NO2↑+O2↑. 2MgO,属于化合反应;(2)2KClO3
2MgO,属于化合反应;(2)2KClO3  2KCl+3O2↑,分解反应;
2KCl+3O2↑,分解反应; 2Ag+2NO2↑+O2↑.
2Ag+2NO2↑+O2↑.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案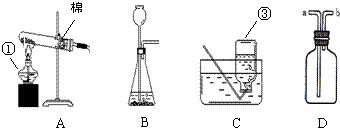 以下是化学实验室内几种常用的实验装置,请回答:
以下是化学实验室内几种常用的实验装置,请回答: