
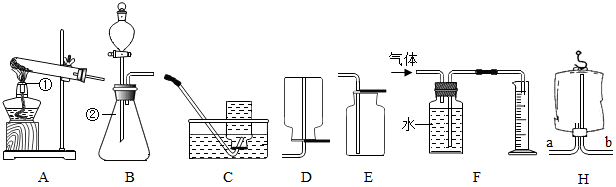
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,向上排空气法收集的氧气干燥,氧气有助燃性,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;
根据二氧化锰是氯酸钾分解的催化剂,可以加快氯酸钾的分解速率进行分析;
(3)根据实验室用高锰酸钾制取氧气时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管进行分析;
(4)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应的反应条件是常温、催化剂进行分析;
(5)根据通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大,其主要原因是:温度没有恢复到室温就开始读数进行分析;
(6)根据氢气密度比空气小进行分析;
(7)根据硫和氧气反应生成的二氧化硫有毒,需要用水吸收进行分析;
(8)根据一氧化氮气体难溶于水,在空气中容易与氧气发生反应进行分析.
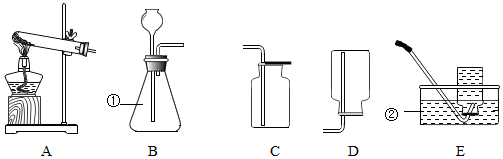
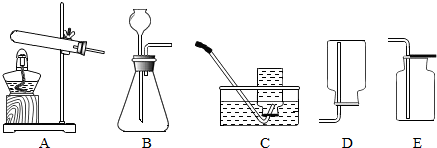
解答 解:(1)通过分析题中所指仪器的作用可知,①是酒精灯,②是锥形瓶;
(2)实验室用氯酸钾制取氧气的反应物是固体,反应条件是加热,所以应选用的发生装置是A,氧气密度比空气大,向上排空气法收集的氧气干燥,所以要收集一瓶干燥的氧气,应选择的收集装置是E,氧气有助燃性,所以检验氧气是否集满的方法是:把带火星的木条放在集气瓶口,木条复燃,证明集满,氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,文字表达式为:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;二氧化锰是氯酸钾分解的催化剂,可以加快氯酸钾的分解速率,所以在加热氯酸钾制取氧气的过程中,发现产生氧气的速率很慢,可能的原因是:没有放催化剂;
(3)实验室用高锰酸钾制取氧气时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管;
(4)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,该反应的反应条件是常温、催化剂,所以该装置的优点是:不用加热;
(5)通过排水量来测定生成氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大,其主要原因是:温度没有恢复到室温就开始读数;
(6)氢气密度比空气小,所以用图H所示医用塑料袋排空气法收集氢气,则氢气导入端为b;
(7)硫和氧气反应生成的二氧化硫有毒,需要用水吸收,所以最好选用气体的收集装置中的C,理由是:二氧化硫有毒,需要用水吸收;
(8)一氧化氮气体难溶于水,在空气中容易与氧气发生反应,所以收集一氧化氮气体时应选用图中装置C,说明一氧化氮已收集满的现象是:集气瓶口有气泡冒出,用该方法收集气体后,发现收集的气体不纯,可能原因是:集气瓶没有装满水.
故答案为:(1)酒精灯,锥形瓶;
(2)A,E,氧气密度比空气大,把带火星的木条放在集气瓶口,木条复燃,证明集满,氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气,没有放催化剂;
(3)需要在试管口放一团棉花,防止高锰酸钾粉末进入导管;
(4)过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,不用加热;
(5)温度没有恢复到室温就开始读数;
(6)b;
(7)C,二氧化硫有毒,需要用水吸收;
(8)C,集气瓶口有气泡冒出,集气瓶没有装满水.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:选择题
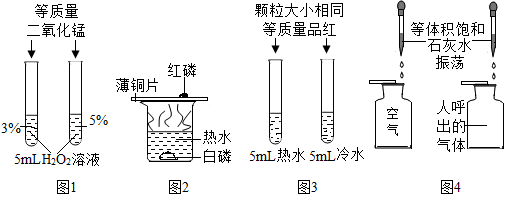
| A. | 图1探究溶液浓度对反应速率的影响 | |
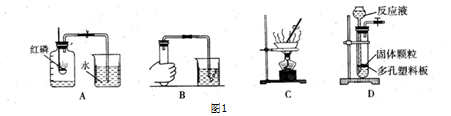
| B. | 图2探究可燃物燃烧的条件 | |
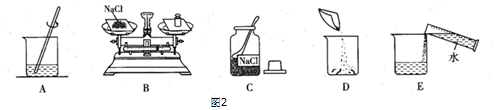
| C. | 图3探究温度对品红扩散速率的影响 | |
| D. | 图4比较二氧化碳含量的多少 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.836 | 5.672 | 8.508 |
| 生成气体的质量/g | 0.100 | 0.200 | 0.250 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属的导电性 | B. | 金属的耐腐蚀性 | C. | 金属的硬度 | D. | 金属的价格 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
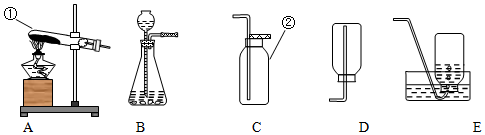
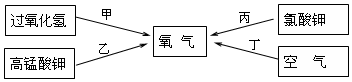
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com