
分析 根据质量守恒定律可知生成氢气的质量就是稀硫酸里溶质硫酸中含有氢元素的质量.
方法一:利用硫酸中氢元素的质量可以计算出稀硫酸中溶质硫酸的质量,再利用溶质质量分数的计算公式即可计算出稀硫酸中溶质的质量分数;
方法二:根据锌与硫酸反应的化学方程式,由生成氢气的质量可以计算出稀硫酸中溶质硫酸的质量,再利用溶质质量分数的计算公式即可计算出稀硫酸中溶质的质量分数.
解答 解:由于稀硫酸与足量的锌完全反应,根据质量守恒定律可知:生成的氢气的质量0.08g就是20g稀硫酸里溶质硫酸中含有的氢元素的质量.故答案为0.08g.
方法一:按化学式计算
稀硫酸中H2SO4质量=$\frac{0.08g}{\frac{2}{98}×100%}$=3.92g
稀硫酸中溶质质量分数=$\frac{3.92g}{20g}$×100%=19.6%
方法二:按化学方程式计算
设20g稀硫酸中溶质质量为x
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.08g
$\frac{98}{x}=\frac{2}{0.08g}$
则x=3.92g;
稀硫酸中溶质的质量分数=$\frac{3.92g}{20g}$×100%=19.6%
答:稀硫酸中溶质的质量分数为19.6%
点评 本题主要考查了质量守恒定律中的元素质量守恒、根据化学式的计算、根据化学方程式的计算和溶质质量分数的计算,难度稍大.


科目:初中化学 来源: 题型:选择题
| A. | 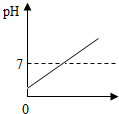 稀盐酸的体积 | B. | 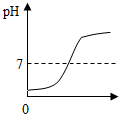 稀盐酸的体积 | C. | 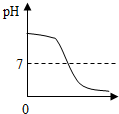 稀盐酸的体积 | D. | 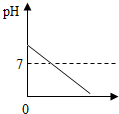 稀盐酸的体积 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 偏左 | B. | 偏右 | C. | 在分度盘的中央 | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
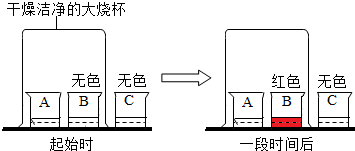
| A. | 水不能使酚酞溶液变红 | B. | 空气不能使酚酞溶液变红 | ||
| C. | 氨分子是运动的而酚酞分子不运动 | D. | 浓氨水易挥发,氨气易溶于水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com