
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验.请计算:
(1)反应后产生气体的质量为 g.
(2)此过氧化氢溶液的溶质质量分数.
科目:初中化学 来源: 题型:计算题
工业上高温煅烧石灰石制取生石灰,发生反应的化学方程式为:CaCO3 CaO+CO2 ↑。若要制取2.8吨生石灰,至少需要含杂质10%(杂质不参加反应)的石灰石多少吨?(结果保留一位小数)
CaO+CO2 ↑。若要制取2.8吨生石灰,至少需要含杂质10%(杂质不参加反应)的石灰石多少吨?(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验.请计算: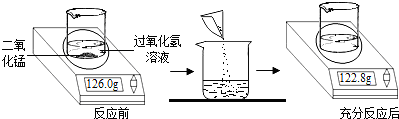
(1)反应后产生气体的质量为 _________ g.
(2)此过氧化氢溶液的溶质质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
汽车尾气排放出的气体主要有NO和NO2,它们污染环境,可用氨气(NH3)除去。
反应的化学方程式为:2NH3 + NO + NO2催化剂 2N2 +3H2O。若反应后得到56g N2,理论
上消耗氨气多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某碱厂的主要产品之一是小苏打(碳酸氢钠),为了测定产品中碳酸氢钠的质量分数(假设该样品中只含氯化钠一种杂质).取样品10.0g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如下图所示.(有关反应:NaHCO3+HCl=NaCl+H2O+CO2↑)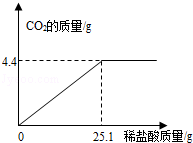
求:(1)样品中碳酸氢钠的质量分数.
(2)恰好完全反应时,所得溶液中溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定某赤铁矿石中氧化铁的质量分数,某化学兴趣小组的同学用过量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用100g氢氧化钠溶液恰好完全吸收,形成不饱和溶液.该溶液总质量与反应时间的变化关系如图.试分析解答:
(1)赤铁矿石中所含主要物质的颜色为: .
(2)实验中多余的一氧化碳能否用水吸收? .
(3)上述反应中产生二氧化碳的质量为 g.
(4)计算实验结束后所得不饱和溶液中所含溶质的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
造纸是我国古代四大发明之一,它有效地推动了人类文明的发展.
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的环境污染.秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为 (用最简整数比表示).
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放.若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可以处理的废水质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“过碳酸钠”(化学式可表示为2Na2CO3?3H2O2)俗称固体双氧水,极易分解,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域.现将一定质量的过碳酸钠粉末溶于m克水中配成稀溶液,再向其中加入适量二氧化锰粉末,充分反应后生成4.8g气体.将反应后的混合物过滤,测得滤液的溶质质量分数为10.6%,求m.(不考虑损耗)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
根据侯德榜制碱法原理,实验室制备纯碱(Na2CO3)的主要步骤是::将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质,经过处理后,转入蒸发皿中,灼烧2小时,得Na2CO3固体。
四种盐在不同温度下的溶解度(g)表
 温度 温度 溶解度 盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | ① | —— | —— | —— |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | —— |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com