
【题目】某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制溶液:
①配制200g8%的氢氧化钠溶液,需水的体积为_____mL(水的密度近似看作1g/cm3)。
②称量时先调节托盘天平平衡,将一只烧杯放在托盘天平的左盘,称量其质量。然后_____(按操作的先后顺序选填字母),直至天平平衡。
A 将氢氧化钠固体加入烧杯中
B 按需要添加砝码、移动游码
③加水充分溶解,并冷却至室温(约20℃)。
(2)用上述配制的氢氧化钠溶液与20g某稀盐酸发生反应的过程中,使用数字传感仪测得溶液温度变化的曲线,如图所示:
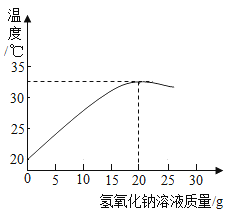
①当加入15g氢氧化钠溶液时,所得溶液中的溶质为_____(用化学式表示)。
②加入_____g氢氧化钠溶液,恰好完全中和。
③试计算此盐酸的溶质质量分数_____。(写出计算过程)
【答案】184 BA NaCl、HCl 20 7.3%
【解析】
(1)①配制200g8%的氢氧化钠溶液,需水的质量=200g×(18%)=184g,这些水的体积=184g÷1g/cm3=184 cm3=184mL,故填18;
②称取氢氧化钠固体时,在称量烧杯质量后,先向天平右盘加入砝码,再移动游码,使砝码与游码的和等于要称量的氢氧化钠的质量数,最后向烧杯中加入氢氧化钠固体,直至天平平衡,即操作的先后顺序为BA,故填BA。
(2)①酸与碱发生的中和反应是一个放热的反应,由图可知,加入15g氢氧化钠溶液时,溶液的温度还没有达到最高温度,即加入的氢氧化钠溶液不足,溶液中还有稀盐酸剩余,则溶液中的溶质有剩余的盐酸和盐酸与氢氧化钠反应生成的氯化钠,其化学式分别是NaCl、HCl,故填NaCl、HCl;
②酸与碱发生的中和反应是一个放热的反应,由图可知,加入20g氢氧化钠溶液时,溶液的温度达到最高温度,即加入的氢氧化钠溶液与盐酸恰好完全反应,故填20;
③解:参加反应的氢氧化钠的质量=20g×8%=1.6g
设氢氧化钠与盐酸恰好完全反应时参加反应的纯HCl的质量为x
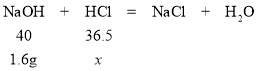
40:36.5=1.6g:x
x =1.46g
此盐酸的溶质质量分数=![]() ×100%=7.3%
×100%=7.3%
答:此盐酸的溶质质量分数为7.3%。


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:
【题目】一碳化学是以分子中只含有一个碳原子的化合物(如CO、CH4等)为原料,合成一系列化工原料和燃料的化学.
(1)煤和高温水蒸气反应可以生成CO和H2 , 反应的化学方程式为________.
(2)天然气的重整可以得到合成气.其微观过程示意图如下所示: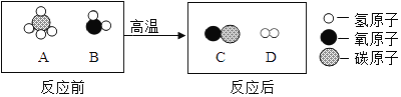
上述物质中,生成物C与D的质量比为________.
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质.仅以合成气为原料不可能得到的物质是_______(填字母序号).
A. 草酸(H2C2O4) B. 甲醇(CH3OH) C. 尿素[CO(NH2)2]
(4)根据下表回答相关问题.
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 (g/100g 水) | KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
①如表中两种物质的溶解度相等的温度范围是在________℃.
②20℃时,硝酸钾的溶解度是________,该温度下,将20gKNO3放入50g水中,充分搅拌,所得溶液的质量是________.要进一步提高该溶液的溶质质量分数,可进行的操作是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像正确的是( )
A.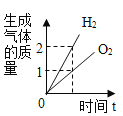 电解水
电解水
B.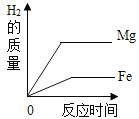 将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中
C.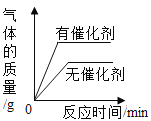 用等体积、等溶质质量分数的过氧化氢溶液制取氧气
用等体积、等溶质质量分数的过氧化氢溶液制取氧气
D.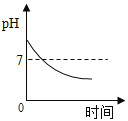 服用胃舒平[主要质量分数的过氧化成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
服用胃舒平[主要质量分数的过氧化成分是Al(OH)3]治疗胃酸过多,胃液pH的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)由于地震和海啸,日本福岛第一核电站发生严重的核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(主要成分是碘化钾KI),以降低放射性碘-131对人体的伤害.
某兴趣小组为了测定某未知碘片中碘化钾的含量,进行了如下图实验:
(查阅资料知:碘化钾易溶于水,而碘化银是不溶于水的黄色沉淀)
![]()
(1)上述步骤③中“物质M”的化学式为 ,其与碘化钾反应的化学方程式是 .
(2)步骤③中“X操作”是 ;该操作与步骤①中的操作都要用到除烧杯外的另一种玻璃仪器,它是 ,它在步骤②中的作用是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( )
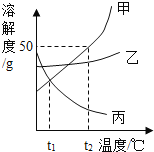
A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液
B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少
C.分别将t2℃时三种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数的大小关系为乙>甲=丙
D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多,丙溶液中无晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)自然界中吸收大气中CO2的最重要环节是_____.
(2)科学家研究得到:海洋是吸收大量CO2的地方.如果CO2排放量继续增加,海洋将被“酸化”.请写出海洋酸化原因的化学方程式________.
(3)科学家目前正在研究将空气中过量的CO2和H2在催化剂和适量条件下转化成液态甲醇和水,反应的化学方程式:CO2+3H2 甲醇+H2O.则甲醇的化学式是______.
甲醇+H2O.则甲醇的化学式是______.
(4)已知20℃时,KCl的溶解度为34克,50℃时的溶解度为42.6克.通过以下实验操作得到溶液①至⑤:
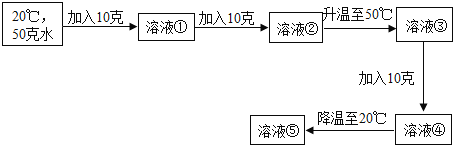
Ⅰ、上述实验所得溶液中,属于饱和溶液的是____;
Ⅱ、溶液④的质量为____克;
Ⅲ、溶液⑤中,溶质的质量分数为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一瓶溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
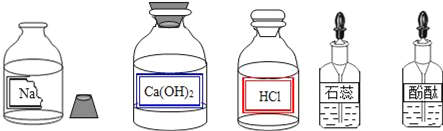
(提出问题)这瓶溶液是什么溶液?
(获得信息)酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
(提出猜想)这瓶溶液是:
猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液.
(实验推断)
(1)小丽取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是__溶液,理由是__;
(2)小刚另取样品滴加稀盐酸有__产生,反应的化学方程式为__,小刚得出结论:该溶液是碳酸钠溶液.
(3)小青认为小刚的结论不完全正确,理由是__.
小组同学讨论后一致认为还需要进行如下实验:
(继续探究)另取样品加入过量的CaCl2溶液,观察到有__产生,设计这一步骤的目的是__;静置后,取上层清液,滴入酚酞试液,溶液呈红色.
(实验结论)这瓶溶液是__.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某化学反应的微观示意图,“![]() ” 、“
” 、“![]() ” 分别表示不同元素的原子,下列有关该反应的说法正确的是()
” 分别表示不同元素的原子,下列有关该反应的说法正确的是()
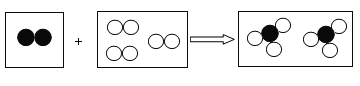
A.该反应属于分解反应
B.反应物和生成物中只有一种单质
C.参加反应的两种元素的化合价反应后均发生改变
D.反应前后原子的种类改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验探究总是能引起同学们的兴趣。某化学兴趣小组在实验室实验时发现了一瓶标签缺损的溶液,如下图。为了确认其溶质成分,同学们进行了如下探究:
(提出猜想)猜想一:NaCl; 猜想二:Na2CO3;猜想三: NaHCO3 猜想四:NaOH
(设计实验一)
小明取少量溶液样品于试管中,用玻璃棒蘸取溶液滴在pH试纸上,读取数据,pH=9,得出结论,猜想四成立。
小王认为小明的结论不准确,理由是:________________。
从小明的实验结果中可以判断出猜想_________也一定是错误的。
(设计实验二)小红取适量稀盐酸于试管中,滴加少量此溶液,溶液中产生气泡。于是认为猜想二正确。
小王认为仍然不能确定,理由是_______________。
(查阅资料)常温下,碳酸钠和碳酸氢钠的溶解度为以下表格中的数据。
Na2CO3 | NaHCO3 | |
溶解度/g | 21.8 | 9.6 |
(分析结论)从资料显示的数据,再结合药品的标签,可以判断猜想_________不正确,理由是_____________________。
(问题交流)(1)Na2CO3和 NaHCO3在生活中被称为“苏打兄弟”,其中NaHCO3在生活中可用来_______________ (写出一条即可)。
(2)Na2CO3在空气中长期放置,会吸收空气中水蒸气和另一种气体而转变成 NaHCO3。请你写出反应方程式________________________。
[注意:若答对以下问题可奖励4分,化学试卷总分不超过60分。]
兴趣小组和老师一起继续实验,将盐酸滴加到Na2CO3溶液中进行反应,并用数字化实验装置pH传感器测定了溶液中pH的变化。采集数据得到曲线如下图所示。
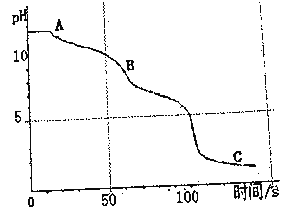
(3)0-50s时,同学们观察到溶液中并没有想象中的气泡产生,请你写出AB段发生反应的化学方程式:__________________。
(4)B点溶液pH大于7,是因为___________(填物质名称)的水溶液呈碱性。
(5)C点所得溶液的溶质是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com