


分析 (1)实验室配制100g溶质质量分数为18%的氯化钠溶液的操作步骤分别是:计算、称量、溶解,根据各操作确定所需要使用的仪器;
(2)根据量筒读数时视线要与凹液面的最低处保持水平,进行分析解答.
(3)根据托盘天平的使用要遵循“左物右码”的原则,进行分析解答.
(4)根据溶液蒸发前后溶质的质量不变,结合题意进行分析解答.
解答 解:(1)配制100g溶质质量分数为18%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶贴签;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒、试剂瓶,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒,故图1中缺少一种玻璃仪器,仪器名称是玻璃棒;用途是搅拌,加快溶解速率.
(2)量取蒸馏水的体积读数如图2所示,则量取的水的体积为82.0mL.
(3)托盘天平的使用要遵循“左物右码”的原则,称量氯化钠的质量读数如图所示,其中正确的是A;B图砝码与药品位置放反了,C图中游码的位置错误.
(4)设要加水的质量为x,根据溶液蒸发前后溶质的质量不变,
则100g×18%=(100g-x)×36% x=50g.
故答案为:(1)玻璃棒;搅拌,加快溶解速率;(2)82.0mL;(3)A;(4)50.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2个氮分子:2N | B. | 2个氮原子:N2 | ||
| C. | 氧化镁中镁元素化合价为+2:$\stackrel{+2}{Mg}$O | D. | 2个氢氧根离子:2OH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 人类的日常生活和工农业生产离不开水和溶液.请回答:
人类的日常生活和工农业生产离不开水和溶液.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
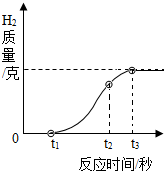 铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡.
铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验目的 | 方法1 | 方法2 | |
| A | 除去铜粉中的铁粉 | 用磁铁吸引 | 加入AgNO3溶液,过滤 |
| B | 鉴别厕所清洁剂和炉具清洁剂 | 加入酚酞溶液,观察现象 | 加入纯碱,观察现象 |
| C | 鉴别二氧化碳和氧气 | 通入CaCl2溶液中,观察 | 伸入燃着的木条 |
| D | 检验氢氧化钠溶液部分变质 | 滴加无色酚酞溶液,观察 | 加入碳酸钠溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
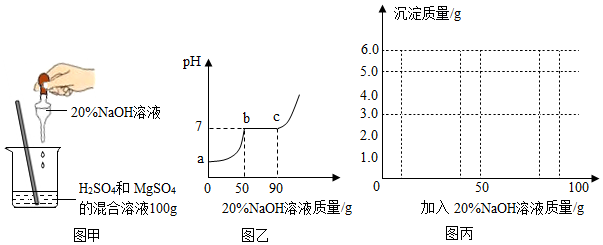
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com