
分析 先假设20g CuO全部反应消耗硫酸质量计算出来,与123.5g×20%所得 H2SO4质量比较,确定出谁过量,再根据不过量的质量计算出生成硫酸铜的质量,再根据20℃时CuSO4的溶解度为20.7g计算出析出的CuSO4•5H2O 晶体的质量.
解答 解:设20g CuO全部反应消耗硫酸质量为X则:
CuO+H2SO4═CuSO4+H2O
80 98
20g X
根据:$\frac{80}{20g}=\frac{98}{X}$
解得X=24.5g,
而123.5g温热的20% H2SO4溶液中含溶质质量为:123.5g×20%=24.7g,所以生成硫酸铜的质量按照20g CuO计算,
设生成硫酸铜质量为Y则:
CuO+H2SO4═CuSO4+H2O
80 160
20g Y
根据:$\frac{80}{20g}=\frac{160}{Y}$
解得Y=40g,
40g硫酸铜结合水的质量设为R:
CuSO4----5H2O
160 90
40g R
根据:$\frac{160}{40g}=\frac{90}{R}$
解得R=22.5g
反应后总溶液质量为:20g+123.5g=143.5g,其中析出晶体后含水质量:143.5g-40g-22.5g=81g,
设这些水中溶解硫酸铜质量为K时达到饱和则:
$\frac{K}{81g}=\frac{20.7g}{100g}$
解得K=16.767g,
则析出硫酸铜质量为40g-16.767g=23.233g,
设析出硫酸铜晶体质量为Z则:
CuSO4---------CuSO4•5H2O
160 250
23.233g Z
根据:$\frac{160}{250}=\frac{23.233g}{Z}$
解得Z=36.3g
故答案为36.3g.
点评 本题容易出错的地方是有的同学按照硫酸去计算生成硫酸铜的质量,忽略了硫酸过量问题.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | 3H--表示三个氢原子 | |
| B. | 3CO2--表示三个二氧化碳分子 | |
| C. | Al3+--表示铝元素的化合价为+3价 | |
| D. | SO2--表示一个三氧化硫分子中含有三个氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ni+H2SO4=NiSO4+H2↑ | B. | Fe+NiSO4=FeSO4+Ni | ||
| C. | Ni+2AgNO3=Ni(NO3)2+2Ag | D. | Cu+NiSO4=CuSO4+Ni |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
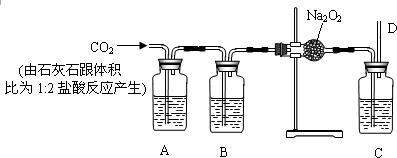
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
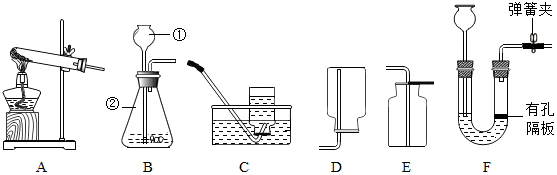
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com