
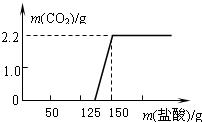
 某研究性学习小组探究实验室中久置的NaOH的变质程度,先称取一定质量的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.
某研究性学习小组探究实验室中久置的NaOH的变质程度,先称取一定质量的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.| 40 |
| 36.5 |
| X |
| 18.25克 |
| 106 |
| 73 |
| Y |
| 36.5克 |


科目:初中化学 来源: 题型:
 某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.查看答案和解析>>
科目:初中化学 来源: 题型:
 34、某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.
34、某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
(10扬州26.) (10分)某研究性学习小组探究CuSO4溶液与NaOH溶液的反应产物。
(1)两溶液混合生成蓝色沉淀的化学方程式是_______。沉淀放置一段时间后,完全变为黑色沉淀,猜想是CuO。为验证猜想,将沉淀过滤、洗涤、烘干后,用CO还原得到红色物质,且生成的气体能使________,写出CO与CuO反应的化学方程式________。
(2)CuSO4溶液与NaOH溶液反应有时也会生成浅绿色沉淀 [化学式为CuSO4·3Cu(OH)2]和Na2SO4,则反应方程式为________。
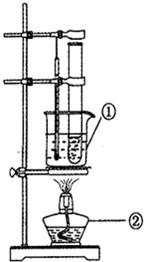
(3)为探究新制Cu(OH),的分解温度,设计水浴加热装置(如图)。
写出仪器的名称:①_______②_______。该装置采用水浴加热,其目的是_______。
(4)18℃时,将溶质质量分数均为10%的CuSO4溶液与NaOH溶液
混合后,测得混合液温度为22℃,说明该反应_____(填“放热”或“吸热”)。当水浴温度分别为30℃、60℃、90℃时,黑色沉淀出现的时间为:2分钟、6秒、1秒,则说明温度越高,Cu(OH)2分解速率越_____(填“快”或“慢”)。该实验说明,Cu(OH)2分解温度________(填“无确定数值”或 “有确定数值”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com