
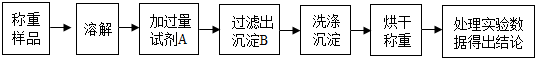
分析 (1)根据银离子和硫酸根离子的性质,硫酸铵和氯化钡反应生成硫酸钡沉淀和氯化铵进行分析;
(2)①根据过滤操作中所需要的仪器分析解答;
②根据氯离子的检验方法来进行解答;
③根据产生的沉淀的质量并结合化学方程式来求算出硫酸铵的质量进而求出氯化铵的质量分数;
④如果沉淀未经洗涤,则在沉淀表面附着着硫酸钠,所以直接烘干导致沉淀的质量增加进行分析.
解答 解:(1)银离子可以和硫酸根结合形成微溶于的物质,而银离子也可以和氯离子反应生成白色沉淀,所以会干扰实验现象的得出,即所选择的试剂A合理的是乙同学,
硫酸铵和氯化钡反应生成硫酸钡沉淀和氯化铵,化学方程式为:(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl;
(2)①为进行过滤操作,准备了以下仪器:烧杯、玻璃棒、铁架台及附件,其中还缺少的一件必备玻璃仪器仪器是漏斗,加入的氯化钡是过量的,所以过滤出沉淀B后滤液中溶质:NH4Cl、BaCl2;
②若沉淀没有洗净,则在洗涤液,存在着氯离子,氯离子可以和银离子生成白色沉淀,所以可以向最后的洗涤液中滴入硝酸银溶液,如果没有白色沉淀产生则说明洗干净了,否则就没洗干净;
③设混合物中硫酸铵的质量为x
(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl
132 233
x 23.3g
$\frac{132}{x}$=$\frac{233}{23.3g}$
x=13.2g
所以氯化铵的质量分数为:$\frac{100g-13.2g}{100g}$×100%=86.8%;
④如果沉淀未经洗涤,则在沉淀表面附着着硫酸钠,所以直接烘干导致沉淀的质量增加,使计算得出的硫酸铵的质量增加,从而使混合物中氯化铵的质量减少,所以计算得到的氯化铵的质量分数偏低.
故答案为:(1)乙,(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl;
(2)①漏斗,NH4Cl、BaCl2;
②取最后的洗涤液,滴加AgNO3溶液,若无沉淀生成,则沉淀已洗净;反之未洗净;
③86.8%;
④偏低.
点评 熟练掌握氯离子和硫酸根离子的鉴别方法,能熟练的书写化学方程式,这是我们进行化学计算的依据,也是我们进行必须掌握的知识点.


科目:初中化学 来源: 题型:选择题
| A. | 加水稀释后CuSO4 溶液颜色变浅 | |
| B. | 观察K2SO4 溶液的颜色 | |
| C. | 向CuSO4 溶液滴加适量的NaOH 溶液,振荡后静置,溶液颜色消失 | |
| D. | 向CuSO4 溶液滴加适量的BaCl2 溶液,振荡后静置,溶液颜色未消失 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
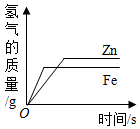 | 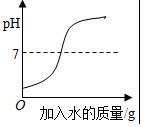 | 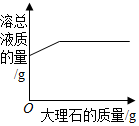 | 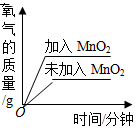 |
| A.等质量的铁和锌与 足量的稀盐酸反应 | B.向一定量的稀硫 酸中加水稀释 | C.向一定量的稀盐 酸中加大理石 | D.等质量、等浓度的 过氧化氢溶液制氧气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
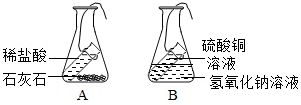
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com