


科目:初中化学 来源: 题型:阅读理解

| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
SO42- SO42- |
加入硝酸钡溶液,若有沉淀则含有该离子 加入硝酸钡溶液,若有沉淀则含有该离子 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:多选题
| A.KNO3、NaCl、Na2SO4 | B.HNO3、NaCl、Na2CO3 |
| C.KOH、Ba(NO3)2、K2SO4 | D.BaCl2、Ca(NO3)2、HCl |
查看答案和解析>>
科目:初中化学 来源:2012年河南省中考化学猜题大赛获奖试卷(解析版) 题型:解答题
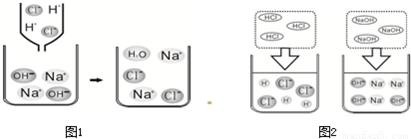
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| ______ | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com