
有如下四种粒子的结构示意图:
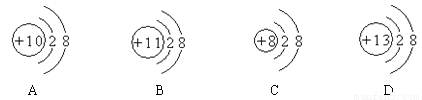
(1)其中属于阴离子的是_________;在化学反应中能够得到电子变成原子的是_________。
(2)下列关于四种粒子的叙述错误的是__________。
A.它们的原子序数不相同
B.它们的核外电子数相同
C.它们都属于金属元素
D.它们都是稳定结构
C BD C 【解析】(1)四种粒子中C的质子数是8,核外电子数是10,8<10,是阴离子;BD中质子数<核外电子数,若能够得到电子则变为原子;(2)A、由图可知:A的质子数是10,即原子序数是10,同理,B、 C、D的原子序数分别是11、8,、13,均不相同,正确;B、四种粒子的核外电子数相同,均是10,正确;C、题给的结构示意图中:A的质子数=核外电子数,最外层电子数是8,是稀有气体元... 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源:广东省江门市2018届九年级下学期第二次模拟考试化学试卷 题型:实验题
请根据如图1回答问题:
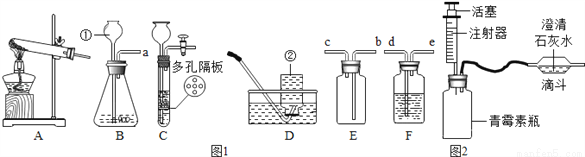
(1)写出仪器的名称:①_______ ②________
(2)用氯酸钾和二氧化锰的固体混合物制氧气,选用的发生装置是______(填A、B或C),反应的化学方程式是_______________,若用E装置收集气体,应从______口通入(填字母).
(3)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置优点是___(答出一点即可)。使用C装置制取二氧化碳,多孔隔板上放的药品应为_______,反应的化学方程式是_______。若用F装置干燥二氧化碳,则F中应装入的液体是______(填名称).
(4)图2是用青霉素瓶、注射器和输液管组成的检验CO32﹣离子的微型实验装置图。用“微型”仪器做实验的优点是______(填序号):
①节约药品用量 ②能完全消除实验污染
③方便个人或家庭实验 ④若需加热也能节约燃料
长颈漏斗; 集气瓶; A; 2KClO32KCl+3O2↑ b; 可以控制反应的发生和停止; 大理石或石灰石; CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸; ①③④; 【解析】(1)①是长颈漏斗方便加液体药品,②是集气瓶是常用的收集气体的仪器; (2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式为2KClO3 2KCl...查看答案和解析>>
科目:初中化学 来源:山东省潍坊市寿光、高密市2018届初三一模化学试卷 题型:综合题
酸、碱、盐在生产生活中具有广泛的用途。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制100g质量分数为10%的氢氧化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为__________g。
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要__________。
③下列操作正确的是__________(填字母序号)。
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1g/cm3)配制100g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为_________g;配制时应选用_________mL的量筒取水(填“100”或“50”或10)。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:

回答下列问题:
①反应Ⅰ的化学方程式为__________________________。
②白色沉淀C是_________________(填化学式)。
③原固体粉末中一定不含________________、______________(填化学式)。
10 量筒 D 50 50 CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ BaSO4 CuSO4 BaCl2 【解析】(1)①需要氢氧化钠固体的质量=100g×10%=10g;②用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、烧杯、玻璃棒、胶头滴管、试剂瓶外,还需要量筒;③A、称量氢氧化钠固体时,应该砝码放在右盘,氢氧化钠放在左边,错误;...查看答案和解析>>
科目:初中化学 来源:山东省潍坊市寿光、高密市2018届初三一模化学试卷 题型:单选题
O2和CO2总与我们如影随形,下列关于它们的叙述中不正确的是
A. 它们都可用向上排空气法收集
B. 空气中O2过多无害,而CO2过多会形成酸雨
C. 自然界里它们可通过光合作用和呼吸作用相互转化
D. O2具有助燃性,而CO2可用来灭火
B 【解析】A、氧气和二氧化碳的密度都比空气的密度大,都可用向上排空法收集,正确; B、氧气具有氧化性,氧气过多会造成氧化过度,CO2过多不会形成酸雨,会引起温室效应,错误; C、二氧化碳是光合作用的原料,氧气是产物;氧气是呼吸作用的原料,二氧化碳是产物,正确; D、氧气能支持燃烧,不能灭火,二氧化碳既不能燃烧也不能支持燃烧,可以灭火,错误。 故选B。查看答案和解析>>
科目:初中化学 来源:重庆市2018届九年级上学期期末考试化学试卷 题型:计算题
硫酸亚铁(FeSO4)常用来作补血剂,绿矾(FeSO4·7H2O)又是一种重要的食品和饲料添加剂。实验室用铁与稀硫酸反应既可以制得硫酸亚铁,也可以制得绿矾。
(1)计算7.6g硫酸亚铁中铁元素的质量___________。
(2)阅读下边的信息提示,列式计算FeSO4·7H2O的相对分子质量__________。

(3)将6g生铁渣加在装有足量稀硫酸的烧杯中,充分反应后,烧杯中物质的总质量减少了0.2g,计算:
①生成硫酸亚铁的质量_________。
②生铁中铁的质量分数____________。
2.8g (56+32+16×4) +7×(1×2+16)=278 15.2 93.3% 【解析】本题考查了相对分子质量的概念及其计算,根据化学反应方程式的计算,化合物中某元素的质量计算 (1)7.6克硫酸亚铁中铁元素的质量为:7.6g× ×100%=2.8g, (2)FeSO4•7H2O的相对分子质量为:(56+32+16×4)+7×(1×2+16)=278, (3)①设...查看答案和解析>>
科目:初中化学 来源:重庆市2018届九年级上学期期末考试化学试卷 题型:单选题
下列方框里是该反应中未列出的一种物质的化学式,实验室可以制得氯气(Cl2)的化学反应是
A. Zn+2HCl=ZnCl2+□
B. □+2NaOH=NaCl+NaClO+H2O
C. Na2CO3+2HCl= 2NaCl+H2O+□
D. MnO2+4HCl(浓) MnCl2+2H2O+□
MnCl2+2H2O+□
查看答案和解析>>
科目:初中化学 来源:重庆市2018届九年级上学期期末考试化学试卷 题型:单选题
下列各组物质中,都由分子构成的是
A. 氧气、氧化汞 B. 金刚石、二氧化碳
C. 硫酸铜、金属铜 D. 氯化钠、氢气
A 【解析】A、氧气属于气态非金属单质,是由氧分子构成的;氧化汞是由氧化汞分子构成的,正确;B、金刚石属于固态非金属单质,是由碳原子直接构成的;二氧化碳是由二氧化碳分子构成的,错误;C、硫酸铜是由铜离子和硫酸根离子构成的;金属铜是金属单质,是由铜原子直接构成的,错误;D、氯化钠是由钠离子和氯离子构成的;氢气属于气态非金属单质,是由氢分子构成的,错误。故选A。查看答案和解析>>
科目:初中化学 来源:内蒙古兴安盟突泉县2018届九年级第一次摸底试卷化学试卷 题型:单选题
五月初五,粽叶飘香,你能闻到香味是因为( )
A.分子在不断运动 B.分子的质量很小 C.分子之间有间隔 D.分子可以再分
A 【解析】 试题分析:分子的基本性质:1、质量、体积都很小,2、在不停地运动且与温度有关,3、分子间存在间隔。五月初五,粽叶飘香,你能闻到香味是因为分子在不断运动,故选A查看答案和解析>>
科目:初中化学 来源:江苏省淮安市2018届九年级下学期第二次调研测试化学试卷 题型:单选题
乙硫醇(化学式为 C2H6S)易挥发,有蒜臭味,人对该气体极其敏感。下列有关乙硫醇的说法不正确的是
A. 乙硫醇的相对分子质量为 62
B. 硫元素的质量分数的计算式是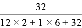 ×100%
×100%
C. 乙硫醇中 C、H、S 三种元素的质量比为 2:6:1
D. 在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏
C 【解析】A、乙硫醇的相对分子质量为12×2+1×6+32=62,故选项说法正确;B、硫元素的质量分数是 ×100%,故选项说法正确;C、乙硫醇中C、H、S三种元素的质量比是(12×2):(1×6):(32×1)≠2:6:1,故选项说法错误;D、乙硫醇易挥发,有蒜臭味,人对该气味极其敏感,在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏,故选项说法正确。故选C。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com