
·ÖĪö æ¼ĀĒŃõ»ÆĆ¾ŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆ¾ŗĶĖ®£¬Ć¾ŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆ¾ŗĶĒāĘų£¬
øł¾ŻÉś³ÉĒāĘųµÄÖŹĮææÉŅŌ¼ĘĖćĆ¾µÄÖŹĮ棬½ųŅ»²½æÉŅŌ¼ĘĖćŃõ»ÆĆ¾µÄÖŹĮ棬“Ó¶ųæÉŅŌ¼ĘĖć·“Ó¦ŗóĖłµĆČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹż£®
½ā“š ½ā£ŗÉčĆ¾µÄÖŹĮæĪŖx£¬²ĪÓė·“Ó¦µÄHClÖŹĮæĪŖy£¬Éś³ÉĀČ»ÆĆ¾µÄÖŹĮæĪŖz£¬
Mg+2HClØTMgCl2+H2”ü£¬
24 73 95 2
x y z 0.2g
Ōņ$\frac{24}{x}=\frac{73}{y}=\frac{2}{0.2g}$=$\frac{95}{z}$£¬½āµĆx=2.4g£¬y=7.3g£¬z=9.5g£®
ŌņÓėŃõ»ÆĆ¾·“Ó¦µÄHClÖŹĮæĪŖ100g”Į14.6%-7.3g=7.3g£®
ÉčŃõ»ÆĆ¾ŗĶĻ”ŃĪĖį·“Ó¦µÄÖŹĮæŃõ»ÆĆ¾ĪŖa£¬Éś³ÉĀČ»ÆĆ¾µÄÖŹĮæĪŖb£®
MgO+2HClØTMgCl2+H2O£¬
40 73 95
a 7.3g b
Ōņ$\frac{40}{a}=\frac{73}{7.3g}=\frac{95}{b}$£¬½āµĆa=4.0g£¬b=9.5g£®
“š£ŗ£Ø1£©Ō»ģŗĻĪļÖŠĆ¾ŌŖĖŲµÄÖŹĮæ·ÖŹż$\frac{2.4g+4.0g”Į£Ø\frac{24}{40}”Į100%£©}{2.4g+4.0g}”Į100%$=75%£»
£Ø2£©·“Ó¦ŗóĖłµĆČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{9.5g+9.5g}{2.4g+4.0g+100g-0.2g}$”Į100%=17.9%£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éѧɜŌĖÓĆ¼ŁÉč·ØŗĶ»Æѧ·½³ĢŹ½½ųŠŠ¼ĘĖćŗĶĶʶĻµÄÄÜĮ¦£¬¼ĘĖ揱ŅŖ×¢Ņā¹ę·¶ŠŌŗĶ×¼Č·ŠŌ£®


 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
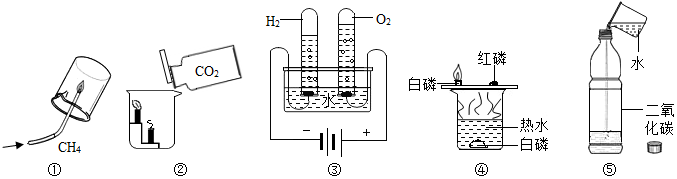
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ū¢Ü¢Ż | D£® | ¢Ł¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
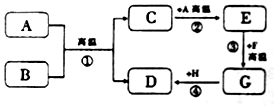 A-H¶¼ŹĒ³õÖŠ»Æѧ֊³£¼ūµÄĪļÖŹ£¬ŅŃÖŖBĪŖŗŚÉ«¹ĢĢ壬DĪŖŗģÉ«¹ĢĢåµ„ÖŹ£¬FĪŖŗģÉ«¹ĢĢ壬ĖüĆĒµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬Ēė»Ų“š£ŗ
A-H¶¼ŹĒ³õÖŠ»Æѧ֊³£¼ūµÄĪļÖŹ£¬ŅŃÖŖBĪŖŗŚÉ«¹ĢĢ壬DĪŖŗģÉ«¹ĢĢåµ„ÖŹ£¬FĪŖŗģÉ«¹ĢĢ壬ĖüĆĒµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2P+5O2ØTP2O5 | B£® | 4Fe+3O2 $\frac{\underline{\;µćČ¼\;}}{\;}$2 Fe2O3 | ||
| C£® | C2H5OH+3O2 $\frac{\underline{\;µćČ¼\;}}{\;}$2CO2+3H2O | D£® | C+2CuO$\frac{\underline{\;øßĪĀ\;}}{\;}$2Cu+CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
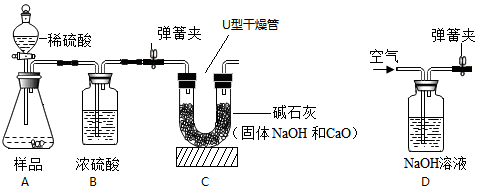
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com