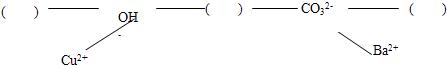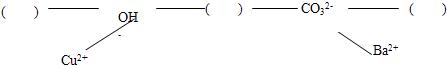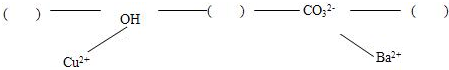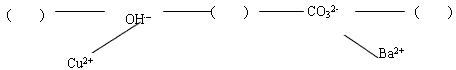同学们在复习完酸碱盐的相关性质后又开展复分解反应研究性学习,进一步从
微观角度探究复分解反应的条件,设计了如下研究性学习思路:
【练习质疑】下列各组物质间均能反应,写出其反应的化学方程式.
①氢氧化钠溶液与硫酸混合
2NaOH+H2SO4=Na2SO4+2H2O
2NaOH+H2SO4=Na2SO4+2H2O
.
②碳酸钠溶液与硫酸混合
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
.
③硫酸铜溶液和氢氧化钠溶液混合
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
.
④氯化钡溶液与稀硫酸混合
BaCl2+H2SO4=BaSO4↓+2HCl
BaCl2+H2SO4=BaSO4↓+2HCl
.
【研究讨论】上述反应为什么能够发生?是因为这些反应物中含有特殊的阴、阳离子,
如①中有H
+和OH
-,②中有H
+和CO
32-,③中有
Cu2+和OH-
Cu2+和OH-
,④中有
Ba2+和SO42-
Ba2+和SO42-
.通过分析,硫酸在反应过程中的实质有所不同,在反应
①②
①②
(填序号)中是硫酸中H
+所表现出来的性质;在反应
④
④
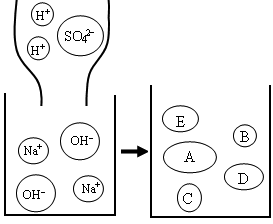
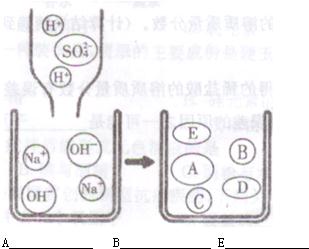
(填序号)中是硫酸根离子表现出来的性质.反应①的微观实质可用下图表示,请填上相关粒子的符号
【构建网络】按照一定的顺序排列这些离子,就可以形成一种网络形式.在网络中,用短线相连的这些阴、阳离子能两两结合生成沉淀或气体或水.现有H
+、Ca
2+、NH
4+,请将它们填入下面合适的“( )”中,使其形成一个更为完整的复分解反应网络