
 小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量(g) | 55.5 | 120.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
分析 (1)分析表格中的数据可以知道11.0g样品最多生成10.0g沉淀,可以据此结合碳酸钠和氯化钙反应的化学方程式进而求算出碳酸钠的质量;
(2)根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图即可完成解答.
(3)烧杯Ⅱ中氯化钠包括原混合物中混有的和碳酸钠与氯化钙反应生成的,再根据质量守恒定律和溶质质量分数计算即可.
解答 解:由实验数据可知,11.0g样品中的碳酸钠与氯化钙溶液充分反应最多生成10.0g碳酸钙.
(1)设要生成10.0g碳酸钙需要碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100117
x 10.0g y
$\frac{106}{x}=\frac{100}{10.0g}=\frac{117}{y}$
解得:x=10.6gy=11.7g
(2)根据图表信息可以知道比较烧杯Ⅰ和烧杯Ⅱ中的数据可以知道,55.5g氯化钙溶液可以和碳酸钠反应生成5.0g沉淀,那么产生10.0g沉淀,所需氯化钙溶液的质量为111.0g,可以据此作图为: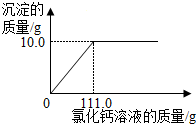
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是:$\frac{11.7g+(11g-10.6g)}{11g+12g-10g}$×100%=10%.
故答案为:
(1)样品中碳酸钠的质量是10.6g;
(2) ;
;
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是10%.
点评 解答这类题目时,首先,要熟记和理解有关含杂质物质的化学反应的有关计算的方法、步骤和格式等相关知识;然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能进行分析计算.


科目:初中化学 来源: 题型:推断题
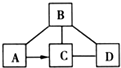 已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)
已知A-D是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐.它们相互间转化或发生反应的关系如图所示.(“-”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系.)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用凹透镜制作近视镜 | |
| B. | 碳酸氢铵不和熟石灰混合施用是为了防止氮元素的损失 | |
| C. | 油锅着火时盖上锅盖是为了隔绝空气 | |
| D. | 热水器安装烟囱是为了防止CO2中毒 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl+NaHCO3═NaCl+CO2↑+H2O | B. | 2HCl+CaS═CaCl2+H2S↑ | ||
| C. | H2S+CuSO4═H2SO4+CuS↓ | D. | 2HCl+CaCO3═CaCl2+CO2↑+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
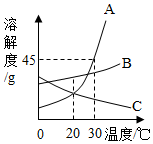 如图是A、B、C三种物质的溶解度曲线,请你根据此图完成下列问题:
如图是A、B、C三种物质的溶解度曲线,请你根据此图完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
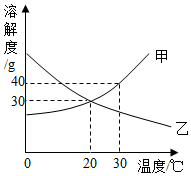 如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeCl2、NaCl、Ba(OH)2 | B. | HCl、Na2CO3、AgNO3 | ||
| C. | Na2SO4、HCl、BaCl2 | D. | KCl、HCl、Al2(SO4)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com