
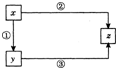
 酸和盐中的三种物质x、y、z,其中有两种元素相同,且这两种元素的质量比均为1:2,其转化关系如图所示:在①②③的转化关系中,一个有气体生成,一个有沉淀生成,一个有沉淀和水生成.则产生的气体可能是________,写出转化②的化学方程式________.
酸和盐中的三种物质x、y、z,其中有两种元素相同,且这两种元素的质量比均为1:2,其转化关系如图所示:在①②③的转化关系中,一个有气体生成,一个有沉淀生成,一个有沉淀和水生成.则产生的气体可能是________,写出转化②的化学方程式________.

科目:初中化学 来源: 题型:
 (2009?十堰)酸和盐中的三种物质x、y、z,其中有两种元素相同,且这两种元素的质量比均为1:2,其转化关系如图所示:在①②③的转化关系中,一个有气体生成,一个有沉淀生成,一个有沉淀和水生成.则产生的气体可能是
(2009?十堰)酸和盐中的三种物质x、y、z,其中有两种元素相同,且这两种元素的质量比均为1:2,其转化关系如图所示:在①②③的转化关系中,一个有气体生成,一个有沉淀生成,一个有沉淀和水生成.则产生的气体可能是查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| OH- | Cl- | SO42- | CO32- | |
| H+ | 溶挥 | 溶 | 溶挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Cu2+ | 不溶 | 溶 | 溶 | 不溶 |
查看答案和解析>>
科目:初中化学 来源:十堰 题型:填空题
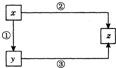
查看答案和解析>>
科目:初中化学 来源:2009年湖北省十堰市中考化学试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com