
 某同学用如图所示的装置测定空气中氧气的体积分数.
某同学用如图所示的装置测定空气中氧气的体积分数. 五氧化二磷.
五氧化二磷.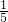 ,由此得出的结论是空气中的氧气约占空气气体的
,由此得出的结论是空气中的氧气约占空气气体的 .
.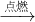 五氧化二磷;(2)烧杯中水进入集气瓶,约占集气瓶剩余容积的
五氧化二磷;(2)烧杯中水进入集气瓶,约占集气瓶剩余容积的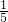 ,空气中的氧气约占空气气体的
,空气中的氧气约占空气气体的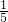 ;(3)与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水偏少;(4)不正确,空气中氧气的含量是一定的;(5)难溶于水、不燃烧、不支持燃烧;(6)不正确,木炭燃烧生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量.
;(3)与室温相比,剩余气体温度较高,压强偏大,因此进入集气瓶中的水偏少;(4)不正确,空气中氧气的含量是一定的;(5)难溶于水、不燃烧、不支持燃烧;(6)不正确,木炭燃烧生成的产物是二氧化碳气体,瓶内压强变化不大,不能测出空气中氧气的含量.

科目:初中化学 来源: 题型:
 20、某无色气体中只含有碳、氧两种元素,一组同学用如图所示的实验来探究该气体的成分,实验中观察到黑色固体逐渐变成红色,澄清的石灰水变浑浊.
20、某无色气体中只含有碳、氧两种元素,一组同学用如图所示的实验来探究该气体的成分,实验中观察到黑色固体逐渐变成红色,澄清的石灰水变浑浊.查看答案和解析>>
科目:初中化学 来源: 题型:
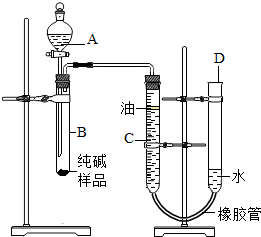 (2012?高淳县一模)小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.
(2012?高淳县一模)小沁同学用如图所示装置测定某纯碱样品(杂质为NaCl)中Na2CO3的质量分数.C为有刻度的玻璃仪器,可装合适的液体,根据液面位置变化测定气体体积.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 某课外活动小组同学用如图所示的装置(固定装置未画出)测定含有杂质的石灰石样品中碳酸钙的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用如图所示的装置(固定装置未画出)测定含有杂质的石灰石样品中碳酸钙的质量分数(杂质与酸接触不产生气体).实验过程是:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
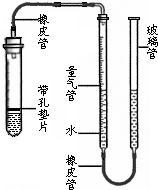 某课外活动小组同学用如图所示的装置(固定装置未画出)测定含有杂质的石灰石样品中碳酸钙的质量分数(杂质与酸接触不产生气体).实验过程是:
某课外活动小组同学用如图所示的装置(固定装置未画出)测定含有杂质的石灰石样品中碳酸钙的质量分数(杂质与酸接触不产生气体).实验过程是:查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省苏州市立达中学九年级(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com