
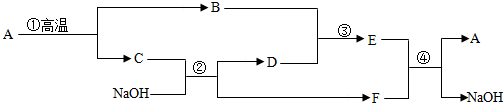
分析 根据D是最常见的溶剂,则D为水,而C能够和NaOH反应生成水和F,则F为钠盐;而E和F(钠盐)反应生成A和NaOH,则E应该是碱,而A必须为不溶性物质才能满足复分解反应的条件.而A可以分解为BC,而B和水能够反应生成可溶性碱,结合碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,则A为碳酸钙,B为氧化钙,C为二氧化碳,E为氢氧化钙,F为碳酸钠;据此进行分析解答.
解答 解:D是最常见的溶剂,则D为水,而C能够和NaOH反应生成水和F,则F为钠盐;而E和F(钠盐)反应生成A和NaOH,则E应该是碱,而A必须为不溶性物质才能满足复分解反应的条件.而A可以分解为BC,而B和水能够反应生成可溶性碱,由碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,则A为碳酸钙,B为氧化钙,C为二氧化碳,E为氢氧化钙,F为碳酸钠.
(1)A的化学为:CaCO3.
(2)反应③,即氧化钙与水反应生成氢氧化钙,该反应符合“多变一”的特征,属于化合反应.
(3)反应④,即碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
故答案为:(1)CaCO3;(2)化合反应;(3)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁试 | 管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还还有的杂质是氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “缺铁性贫血”里所说的铁不是单质铁 | |
| B. | 家用铝锅不可以用来盛放酸性食物 | |
| C. | 水可用来鉴别硝酸钾固体和氢氧化钠固体 | |
| D. | 铁丝和铜丝分别插入氢氧化钠溶液中,都无变化,说明铁和铜一样不活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
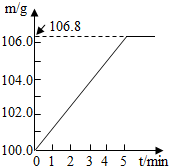 某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸完全吸收.测得吸收氨气后溶液总质量m与反应时间t的变化如图所示.所涉及的反应为:
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸完全吸收.测得吸收氨气后溶液总质量m与反应时间t的变化如图所示.所涉及的反应为:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | Fe(Cu) | 加过量FeSO4溶液、过滤 |
| B | CaO(CaCO3) | 加足量的水、过滤 |
| C | NaCl溶液(Na2CO3) | 加入适量的CaCl2溶液、过滤 |
| D | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淀粉遇加碘食盐溶液会变蓝 | |
| B. | 瘦肉中主要含蛋白质,不含无机盐之类的营养素 | |
| C. | 某气体能使灼热的氧化铜还原成铜,这种气体一定是一氧化碳 | |
| D. | 鉴别氢氧化钠固体和硝酸铵固体,可加适量水溶解,用手触摸试管外壁温度的变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
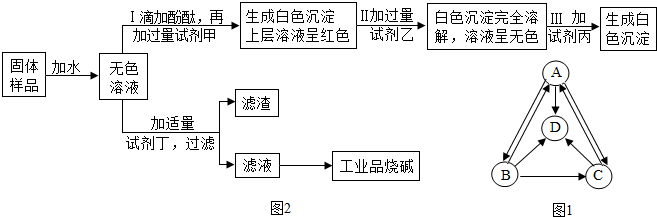
| 实验步骤 | 实验现象 |
| Ⅰ.向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ.向样品溶液中滴加稀硫酸, 并用玻璃棒搅拌 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com