
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示。
⑴当加入NaOH溶液质量为ag时,溶液中的溶质有 ;
⑵求混合溶液中CuCl2的质量分数。
⑶求恰好完全反应时,消耗NaOH溶液的总质量。

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
某同学郊游时不慎被蜜蜂蛰伤,蜜蜂的刺液是酸性的。为减轻疼痛可以在蛰伤处涂抹( )
A.食醋(pH≈2) B.牛奶(pH≈6.5)
C.矿泉水(pH≈7) D.肥皂水(pH≈10)
查看答案和解析>>
科目:初中化学 来源: 题型:
以下推理正确的是 ( )
A. 酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B. 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性
C. 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D. 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
查看答案和解析>>
科目:初中化学 来源: 题型:
在初中阶段,我们已经学习了利用某些仪器和药品制取气体,下图所示A—E装置可供实验室制取有关气体时选用。

(1)写出图中有标号仪器的名称:a ;
(2)实验室用大理石和稀盐酸制取CO2可选用的发生装置和收集装置是 ;该反应的化学方程式是 。学科王
(3)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,可用加热氯化铵和氢氧化钙的固体混合物制取。如果要制取氨气你应选择的发生装置和收集装置是 。为验证氨气的部分性质,将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到两种现象:①滴有酚酞的水会进入集气瓶中,② 。
查看答案和解析>>
科目:初中化学 来源: 题型:
下列化学方程式书写正确的是( )
|
| A. | C+O2 | B. | Zn+H2SO4═ZnSO4+H2 |
|
| C. | 4Fe+3O2 | D. | C+CuO |
查看答案和解析>>
科目:初中化学 来源: 题型:
下列反应中属于置换反应的是( )
A. 3Fe+2O2
 Fe3O4 B.
Fe3O4 B. 2H2O
2H2O
 2H2↑+O2↑
2H2↑+O2↑
C. Fe+CuSO4
 FeSO4+Cu D. NaOH+HCl
FeSO4+Cu D. NaOH+HCl
 NaCl+H2O
NaCl+H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
pH是水质检验的重要指标之一。下列水样中,酸性最强的是
A.pH = 1.3的工业废水 B.pH = 4.5的 雨水
雨水
C.pH = 7.0的蒸馏水 D.pH = 7.3的矿泉水
查看答案和解析>>
科目:初中化学 来源: 题型:
小亮同学想通过实验探究某企业采用的氨碱法制的的纯碱样品的成分及含量。
【提出问题1】该纯碱样品中含有哪些 物质?
物质?
【猜想与假设】通过分析,小亮做出如下假设:
(1)只含有Na2CO3 ; (2)含有Na2CO3和NaHCO3
【查阅资料】
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 产生气泡 | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(1)现象Ⅱ对应的化学方程式为 。
【实验探究】为了确定纯碱样品的成分,小亮设计如下实验方案,请你一起完成小列实验报告。
| 实验步骤 | 实 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液。 | ; | 氯化钙溶液过量的目的是 。 |
| ②将上述反应后的混合液过滤,取滤液 。 | ; | 证明猜想②成立。 |
【提出问题2】如何测量该纯碱样品中各物质的含量?
(1) 为测量该纯碱样品各成分的含量,小亮设计了右图装置,通过称量B装置的质量变化来确定样品中各成分的含量。该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差。造成偏差的原因有① ;
 ② 。
② 。
(2) 小亮在老师的指导下重新设计了如下的实验装置。该实验有以下操作步骤:
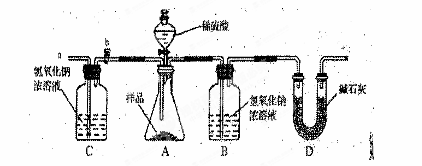
①检查装置气密性,将9.5 g 干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
 ⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量。
该实验的正确步骤是  。
。
【计算】实验完毕后测得 B装置增重4.4g,则样品中各成分的质量分别为多少?(写出计算过程)
B装置增重4.4g,则样品中各成分的质量分别为多少?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com