
 某化学活动小组在复习了硫酸的有关知识后,请你作为该小组成员做如下的归纳整理:
某化学活动小组在复习了硫酸的有关知识后,请你作为该小组成员做如下的归纳整理:分析 (1)浓硫酸具有吸水性,可以用作某些物质的干燥剂;
(2)稀硫酸显酸性,能使石蕊试液变红色;
酸能和碱反应生成盐和水;
氧化铁和稀硫酸反应生成硫酸铁和水;
碳酸钠能和稀硫酸反应生成硫酸钠、水和二氧化碳;
为了比较镁和锌与稀硫酸反应的快慢,金属的形状、稀硫酸的质量分数、温度等都要相同
解答 解:(1)浓硫酸有吸水性,常作某些气体的干燥剂.
故填:吸水.
(2)I.为了验证性质①,小英将紫色石蕊试液滴加到稀硫酸中,溶液变红色.
故填:红.
Ⅱ.图中A所表示的物质类别是碱.
故填:碱.
Ⅲ.为了验证性质⑤,可选用的物质是碳酸钠,因为碳酸钠能和稀硫酸反应生成硫酸钠、水和二氧化碳.
故填:碳酸钠.
IV.镁和锌可以用来验证性质②,小英要探究镁和锌与稀硫酸反应的快慢,需要控制不变的量是两种金属的形状、稀硫酸的质量分数和温度.
故填:ABD
点评 酸具有一些相似的化学性质,例如能和酸碱指示剂反应,能和某些金属单质、某些金属氧化物、某些盐反应,能和碱反应生成盐和水.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
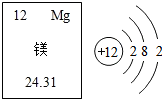 打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;
打造更完美的电动汽车,镁电池或将取代锂电池成新一代霸主.(1)元素的相对原子质量为24.31;查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 坚决取缔马路烧烤 | B. | 开发太阳能等新型能源 | ||
| C. | 提倡使用一次性餐具 | D. | 大力发展公共交通 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,把浓硫酸慢慢注入盛有水的量筒中,并不断搅拌 | |
| B. | 用天平称量氢氧化钠固体时,放在左盘的纸上称量 | |
| C. | 浓硫酸不慎粘到皮肤上应用大量水冲洗,然后涂上3%~5%的氢氧化钠溶液 | |
| D. | 点燃氢气等可燃性气体前,一定要检验气体的纯度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热碳酸氢钠固体,得到白色碳酸钠固体 | |
| B. | 硫在氧气中燃烧,发出淡蓝色火焰 | |
| C. | 灼烧棉纱线,产生烧焦羽毛的气味 | |
| D. | 电解水时,正极得到能使带火星的木条复燃的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com