
今有氢氧化钠、碳酸氢钠和与其他物质都不反应,受热也不分解的杂质组成的固体混合物17.110g,放入密闭容器中加热至250℃,经充分反应后,将容器中的气体通入过量的澄清石灰水中得到白色沉淀2.500g;当容器中的残留固体冷却到室温后,全部溶于水制成50.00ml溶液,从中取出10.00ml,恰好可与含HCl 1.825g的盐酸溶液25.00毫升中和至中性,求原混合物中含杂质的质量分数?
2.98%
【解析】
试题分析:氢氧化钠、碳酸氢钠放入密闭容器中加热至250℃,氢氧化钠与碳酸氢钠反应生成碳酸钠和水,过量的碳酸氢钠分解生成碳酸钠、水和二氧化碳;生成的二氧化碳与能澄清石灰水生成碳酸钙沉淀,因此,利用沉淀碳酸钙的质量可计算放出气体二氧化碳的质量,再由二氧化碳的质量可计算出分解的碳酸氢钠的质量及生成的碳酸钠的质量;根据溶液的均一性,从50mL溶液取出10mL溶液时,溶液中溶质质量也为原溶质质量的五分之一;碳酸钠溶液呈碱性,与盐酸完全反应生成氯化钠和水,溶液呈中性;利用反应消耗盐酸的质量计算出加热后残留固体中碳酸钠的质量,用其质量减去碳酸氢分解产生的碳酸钠,所得碳酸钠质量即为氢氧化钠与碳酸氢钠反应所生成碳酸钠质量,由此计算混合物中氢氧化钠与碳酸氢钠的质量;最后使用混合物的质量减去氢氧化钠和碳酸氢钠的质量即可求得混合物中杂质质量,杂质质量与混合物质量比求出混合物中所含杂质的质量分数。
由题意可知NaHCO3过量,NaOH与CO2反应和NaOH与NaHCO3直接反应所生成的Na2CO3总质量是不变的,取NaHCO3计算更简便,有关反应如下:
NaOH+NaHCO3=Na2CO3+H2O ①
2NaHCO3 Na2CO3+CO2↑十H2O↑ ②
Na2CO3+CO2↑十H2O↑ ②
CO2+Ca(OH)2=CaCO3↓+H2O ③
Na2CO3+2HCl=2NaCl+H2O+CO2↑ ④
(1)设反应②分解的NaHCO3质量为x,分解产生的Na2CO3质量为y,由②③有:
2NaHCO3~Na2CO3~CaCO3
168 106 100
x y 2.500g
x= = 4.200g y=
= 4.200g y= = 2.650g
= 2.650g
(2)残留物全部中和至中性需HCl的质量为: ×50.00毫升 = 9.125g
×50.00毫升 = 9.125g
设残留物中Na2CO3的总质量为z,由④有:
Na2CO3~2HCl
106 73
z 9.125g
 =
=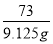 z=13.250g
z=13.250g
反应④产生的Na2CO3质量为 13.250g—2.650g=10.600g
10.600克Na2CO3是原混合物中的NaOH(设质量为a)和除发生分解反应之外的NaHCO3(设质量为b)恰好反应生成的,它们的质量关系是:
NaOH~NaHCO3~Na2CO3
40 84 106
a b 10.600g
a=4.00g, b=8.400g
杂质的质量分数为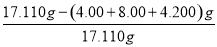 ×100% ≈ 2.98%
×100% ≈ 2.98%
答:略
考点:根据化学反应方程式的计算;酸的化学性质;碳酸钠、碳酸氢钠与碳酸钙;质量守恒定律及其应用


科目:初中化学 来源:2013-2014学年重庆市九年级下学期第一次诊断考试化学试卷(解析版) 题型:选择题
根据右图的信息判断,下列说法正确的是( )

A.硫属于金属元素
B.硫原子的相对原子质量为32.07 g
C.硫原子的核电荷数为16
D.在化学反应中,硫原子容易失去电子
查看答案和解析>>
科目:初中化学 来源:2013-2014学年辽宁省丹东市九年级第一次模拟考试化学试卷(解析版) 题型:选择题
化学与生活息息相关。
(1)家用食醋pH应 7,向食醋中滴加几滴酚酞试液后,再滴加氢氧化钠溶液至过量,观察到的现象是 。
(2)空气是由多种气体组成,它属于 (选填“混合物”或“纯净物”),植物的光合作用是空气中 的主要来源。
(3)锅里的油一旦着火,可用锅盖盖灭,其原理是 ;
(4)煤、 、天然气称为化石燃料,天然气的主要成分为甲烷。
甲烷在空气中燃烧的化学方程式 。
(5)稀土元素铕是激光及原子能应用的重要材料。已知三氯化铕的化学式为EuCl3,则氧化铕的化学式为 。
(6)户外探险缺少饮用水,可将浑浊的河水用简易净水器进行净化,其中加入的活性炭是利用它的 性。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年贵州省黔东南地区九年级模拟测试(六)化学试卷(解析版) 题型:填空题
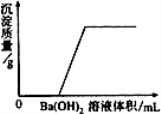
某溶液由NaOH、KNO3、HCl、H2SO4和MgCl2中的一种或几种组成。向该溶液中滴加Ba(OH)2 溶液,产生沉淀的质量与加入Ba(OH)2 溶液体积的关系如右图所示。请你从图中获得的信息来分析,该溶液中不可能存在的物质是 ;肯定存在的物质是 。可能存在的是 。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年贵州省黔东南地区九年级模拟测试(六)化学试卷(解析版) 题型:选择题
如图为甲、乙两种固体物质在水中的溶解度曲线。

下列说法正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.在t1℃时,甲、乙两物质溶液溶质质量分数相等
C.在t2℃时,H点表示乙物质的不饱和溶液
D.由t1℃升温到t2℃时,甲物质溶液溶质质量分数不变
查看答案和解析>>
科目:初中化学 来源:2013-2014学年福建省化学竞赛模拟化学试卷(解析版) 题型:填空题
有多种方法可以鉴别氯化钠和碳酸钠两瓶无色溶液。请用两种方法区别氯化钠和碳酸钠两瓶无色溶液(要求说明实验方法、观察到的现象和结论)。
(1) ;
(2) 。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年福建省化学竞赛模拟化学试卷(解析版) 题型:填空题
已知Ba2+一旦被人体吸收进入血液会使血液中的蛋白质凝结,造成中毒,危及生命。然而,BaSO4却能用作X光造影诊断胃肠疾病的“钡餐”,原因是BaSO4的溶解性极小,产生Ba2+的量极微,不足以对人体造成危害。BaCO3也是难溶物质,但它绝对不能替代BaSO4作为“钡餐”,否则会造成中毒,原理用化学方程式表示为 ,若误服BaCO3,可服用MgSO4进行解毒原理用化学方程式表示为 。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年福建省化学竞赛模拟化学试卷(解析版) 题型:选择题
下列四种离子:Fe2+、H+、Cu2+、Hg2+,在溶液中转变成原子的能力,由强到弱的顺序正确的是( )
A.Fe2+>H+>Cu2+> Hg2+ B.Hg2+>Cu2+>H+> Fe2+
C.H+> Fe2+> Hg2+>Cu2+ D.Cu2+> Hg2+> Fe2+>H+
查看答案和解析>>
科目:初中化学 来源:2013-2014学年湖北省黄冈市九年级下学期入学考试化学试卷(解析版) 题型:填空题
实验室制取气体常常用到下列装置,根据给出的装置回答下列问题:

(1)写出标号仪器的名称:① ;
(2)若该实验选择装置A来制取氧气,请写出该反应的化学方程式 。用C装置收集氧气,判断氧气已收集满的现象是 。
(3)某同学从上述装置图中选用适当装置成功的制备和收集了二氧化碳,选用的装置是
(填字母).为了进一步验证产生的气体是二氧化碳,该同学将气体通入图F装置中,则F装置中应加入的试剂为 (填化学式).
(4)若要制取氢气,用F装置收集,气体应从 (填“a”或“b”)导管口通入。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com