
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶解,再加入 | 乙的猜想 不成立 | |
| 2 | 取步骤1反应后的溶液于试管中 | 无明显现象 | 只有甲的 猜想成立 |
| 106 |
| 73 |
| X |
| 200g×7.3% |
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶解,再加入过量的氯化钙溶液 | 生成白色沉淀 | 乙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中滴加无色酚酞试液 | 无明显现象 | 只有甲的 猜想成立 |
| 106 |
| 73 |
| X |
| 200g×7.3% |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
| A、离子是带电的粒子,则带电的粒子一定是离子 |
| B、氧化物中含有氧元素,则含有氧元素的化合物一定是氧化物 |
| C、某物质燃烧生成CO2和H2O,则该物质中一定含碳、氢元素 |
| D、燃烧一般都伴随发光和放热现象,则有发光和放热现象的变化都是燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
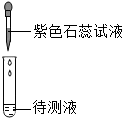 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.| 操作方法 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
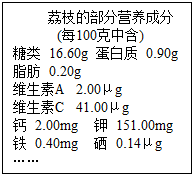 荔枝是很多人喜爱的水果,其中含有丰富的营养成分,如图所示.请回答:
荔枝是很多人喜爱的水果,其中含有丰富的营养成分,如图所示.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用水鉴别碳酸钙和氯化钠两种固体 |
| B、用稀盐酸除去铁粉中混有的少量铜粉 |
| C、用浓硫酸除去氧气中混有的少量水蒸气 |
| D、用紫色石蕊溶液鉴别二氧化碳和一氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com