
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取上述少量氢氧化钠固体溶于水配成溶液,向溶液中滴加BaCl2溶液至过量,充分反应后,静置 | 产生白色沉淀 | 说明久置的氢氧化钠固体中,一定含有Na2CO3(填化学式) |
| 步骤二:用玻璃棒蘸取少量步骤一中的上层清液,滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置的氢氧化钠固体中,还一定含有NaOH(填化学式) |
分析 【实验方案】
根据碳酸钠溶液能与BaCl2溶液反应生成碳酸钙沉淀,可据有沉淀生成判断溶液中含有碳酸钠;加入过量的BaCl2溶液除掉了碳酸钠后,溶液显碱性,说明了溶液中还含有氢氧化钠;根据碳酸钠溶液能与BaCl2溶液反应生成碳酸钙,来检BaCl2溶液是否过量;
【实验结论】综合上述实验现象可知猜想Ⅱ正确;
【反思】运用氢氧化钠和二氧化碳反应生成碳酸钠和水书写方程式;
解答 解:【实验方案】
由于BaCl2溶液能与碳酸钠溶液反应生成碳酸钙,所以根据二者混合后有沉淀生成可推出溶液中含有碳酸钠;加入过量的BaCl2溶液是为了除掉碳酸钠,pH=11,说明溶液仍然显碱性,说明了溶液中还含有氢氧化钠;
【实验结论】综合以上实验可知久置固体中有氢氧化钠和碳酸钠,猜想二正确;
【反思】氢氧化钠溶液变质是由于和空气中的二氧化碳发生反应生成了碳酸钠的缘故,该反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O,氢氧化钠要密封保存;
【故答案为:
【实验方案】
Na2CO3;NaOH;除去Na2CO3;
【实验结论】二;
【反思】CO2+2NaOH═Na2CO3+H2O;密封;
点评 本题探究了氢氧化钠的变质情况,有关实验方案的设计和对实验方案的评价是中考的热点之一,掌握碱的有关性质,碳酸根离子的检验是解答本题的关键.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油锅着火立即用水扑灭 | B. | 用燃烧的方法鉴别蚕丝和涤纶 | ||
| C. | 用钢丝球擦洗铝壶上的污垢 | D. | 煤气泄漏,及时打开换气扇排气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
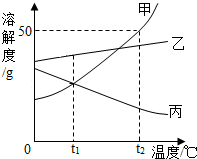
| A. | t2℃时,把50g甲放入50g水中得到甲的饱和溶液,且溶液的溶质质量分数为50% | |
| B. | t1℃时三种物质的溶解度大小顺序是乙>甲=丙 | |
| C. | 将t2℃时等质量的三种物质的饱和溶液分别降至0℃,析出甲最多 | |
| D. | 将丙的饱和溶液变为不饱和溶液,可以采用降温的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| OH- | NO3- | Cl- | SO42- | |
| H + | - | 溶、挥 | 溶、挥 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 溶 | 溶 | 溶 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com