
| ||
| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A | 物质的性质与用途 | B | 安全常识 |
| N2性质稳定--填充食品袋防腐 O2支持燃料--可作火箭燃料 石墨很软--可作电极 |
煤气泄漏--打120报警 煤矿爆炸--由瓦斯引起 假盐中毒--由NaNO2引起 | ||
| C | 日常生活经验 | D | 元素与人体健康 |
| 除去餐具上的油渍-用洗涤剂清洗 鉴别羊毛、涤纶-点燃嗅闻气味 使煤燃烧更旺--把煤做成蜂窝状 |
缺碘-易甲状腺肿大 缺维生素C-易引起贫血 缺钙-易骨质疏松或得佝偻病 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
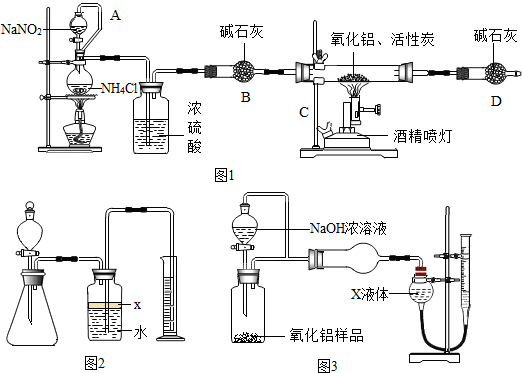
| ||
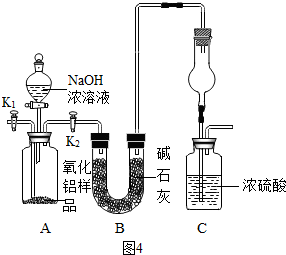
查看答案和解析>>
科目:初中化学 来源: 题型:
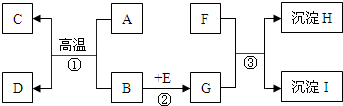
查看答案和解析>>
科目:初中化学 来源: 题型:
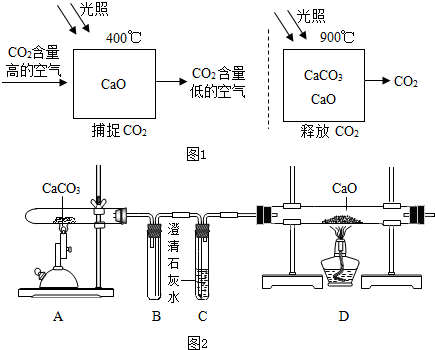
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想Ⅱ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
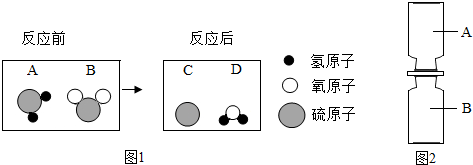
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
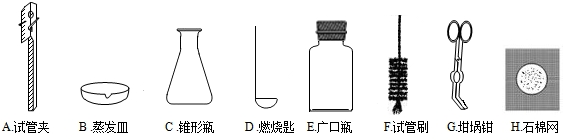
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com