
分析 每个氧分子由2个氧原子构成;
氮元素的元素符号可以表示氮元素;
稀有气体都是由单原子构成的分子;
每个硫酸根离子带2个单位负电荷;
每个钙离子带2个单位正电荷;
元素的化合价应该标在元素符号的正上方.
解答 解:(1)两个氧分子可以表示为2O2;
(2)三个氮原子可以表示为3N;
(3)氩气可以表示为Ar;
(4)三个硫酸根离子可以表示为3SO42-;
(5)两个钙离子可以表示为2Ca2+;
(6)氧化铜中铜为正二价,可以表示为$\stackrel{+2}{Cu}$O.
故填:2O2;3N;Ar;3SO42-;2Ca2+;$\stackrel{+2}{Cu}$O.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.


科目:初中化学 来源: 题型:解答题
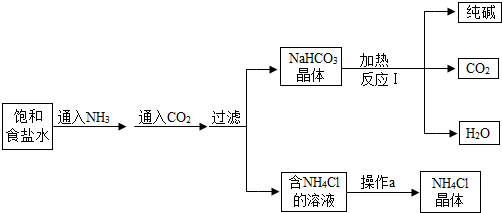
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反氢原子呈电中性 | B. | 1个反中子带1个单位负电荷 | ||
| C. | 反氧原子核外有8个反电子 | D. | 反原子的质量主要集中在原子核上 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组的同学用如图所示的实验探究分子的运动,请回答下列问题:
某化学兴趣小组的同学用如图所示的实验探究分子的运动,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.
氯化钾和硝酸钾晶体在不同温度时的溶解度如下表所示.| 0 | 10 | 20 | 30 | 40 | |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
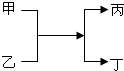 甲、乙、丙、丁均为初中化学常见物质,它们有如图的转化关系,请回答:
甲、乙、丙、丁均为初中化学常见物质,它们有如图的转化关系,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com