
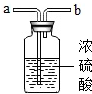
 已知碳酸氢钠加热能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解.现有某工厂生产出的一批碳酸氢钠中混有少量的碳酸钠,取4.0g 样品加热到质量不再减少时,共收集到二氧化碳气体0.88g.
已知碳酸氢钠加热能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解.现有某工厂生产出的一批碳酸氢钠中混有少量的碳酸钠,取4.0g 样品加热到质量不再减少时,共收集到二氧化碳气体0.88g.
| ||
| ||
| 168 |
| x |
| 44 |
| 0.88g |
| 4.0g-3.36g |
| 4.0g |
| ||


科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的 |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有 |
| 实验操作 | 实验现象 | 实验结论 |
| ①将久置固体研碎,然后用磁铁吸引 ②将吸引后剩余的固体加入方管中,加入适量稀盐酸 ③将生成的气体通入澄清石灰水 |
①固体减少,有气泡冒出,溶液变为黄色. ② |
固体中一定含有CaCO3和 |
查看答案和解析>>
科目:初中化学 来源: 题型:
A、Mg+O2
| ||||
B、H2O
| ||||
C、4Fe+3O2
| ||||
D、2KMnO4
|
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、该物质属于氧化物 |
| B、该物质中碳、氢、氧的质量比为3:4:3 |
| C、该物质的相对分子质量为176 |
| D、其分子由碳原子、氢分子和氧分子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、Na2SO4、FeCl3、NH4NO3、NaNO3 |
| B、Na2CO3、NaCl、NH4Cl、CuSO4 |
| C、Na2SO4、NaCl、NH4NO3、(NH4)2SO4 |
| D、Na2CO3、H2SO4、BaCl2、KNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 操作 | 现象 | 结论 |
| 取少量两种滤液分别于两支试管中,滴加少量 |
优质珍珠粉的滤液没有变色;廉价“珍珠粉”的滤液变红 | 猜想①成立 |
| 取少量两种滤液分别于两支试管中,加入一定量 |
优质珍珠粉的滤液有黄色出现,局部变黑;廉价“珍珠粉”的滤液没有明显现象 | 猜想②成立 |
| 优质珍珠粉 | 廉价“珍珠粉” | |
| 固体粉末的质量 | 10.00g | 10.00g |
| 加入稀盐酸的质量 | 46.00g | 50.13g |
| 反应后烧杯中物质的质量 | 52.00g | 55.77g |
查看答案和解析>>
科目:初中化学 来源: 题型:
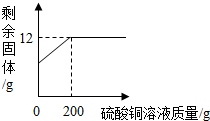 某兴趣小组想探究某生铁中铁的质量分数,现取两份质量和组成一样的生铁样品,一份与稀盐酸混合,一份与硫酸铜溶液混合,杂质不溶于水,也不参加化学反应,得到相关数据如表(图):
某兴趣小组想探究某生铁中铁的质量分数,现取两份质量和组成一样的生铁样品,一份与稀盐酸混合,一份与硫酸铜溶液混合,杂质不溶于水,也不参加化学反应,得到相关数据如表(图):| 加入稀盐酸的质量/g | 20 | … | 60 |
| 剩余固体质量/g | 8 | … | 0.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
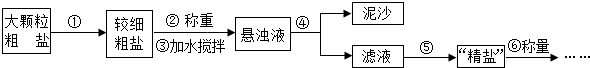
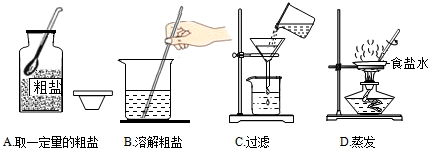
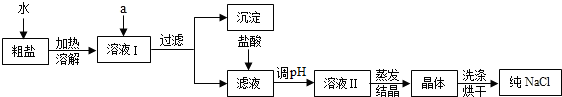
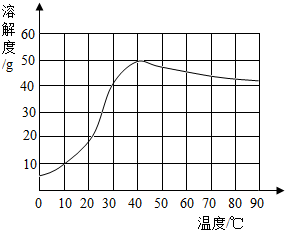
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com