考点:实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,燃烧与燃烧的条件
专题:综合实验题
分析:(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰做催化剂,故可书写其化学方程式,D中稀盐酸和石灰石可反应生成二氧化碳,据此解答;
(2)B中白磷能够燃烧的原因,应考虑燃烧的条件;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;
(4)用F装置是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大,验满二氧化碳的方法是将燃烧的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)据石灰石和稀盐酸反应原理书写方程式,据反应特点分析反应类型;
(6)稀硫酸和石灰石反应生成微溶性的硫酸钙,会覆盖在石灰石表面,阻止反应的进行.
解答:解:(1)由题意知,反应物双氧水,生成物水和氧气,反应条件为二氧化锰,故方程式是2H
2O
22H
2O+O
2↑;D中稀盐酸和石灰石可反应生成二氧化碳,所以会看到石灰石表面有气泡产生;
(2)B中白磷能够燃烧的原因是白磷的温度达到着火点,与氧气接触;
(3)二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色;反应的化学方程式为:CO
2+H
2O=H
2CO
3;
(4)用F装置是向上排空气法,适合收集密度比空气大的气体,故收集气体的依据是气体密度比空气密度大,F中收集的气体是二氧化碳,要检验二氧化碳是否收集满的方法是:将燃烧的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)盐酸压入D和石灰石反应生成二氧化碳、水和氯化钙,反应的化学方程式为:CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑,该反应是由两种化合物互相交换成分生成氯化钙、碳酸,碳酸不稳定分解生成水和二氧化碳,属于复分解反应;
(6)稀硫酸和石灰石反应生成微溶性的硫酸钙,会覆盖在石灰石表面,阻止反应的进行,所以制备二氧化碳不能用稀硫酸;
故答案为:
(1)2H
2O
22H
2O+O
2↑;石灰石表面有气泡产生;
(2)温度达到着火点,与氧气接触;
(3)紫色石蕊试液变红;CO
2+H
2O=H
2CO
3;
(4)气体密度比空气密度大;将燃烧的木条放于集气瓶口,若木条熄灭,说明收集满了;
(5)CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑;
(6)不可以;稀硫酸和石灰石反应生成微溶性的硫酸钙,会覆盖在石灰石表面,阻止反应的进行.
点评:掌握氧气的反应原理、制取和收集方法;掌握二氧化碳的实验室制法及其物理性质和化学性质;注意燃烧与燃烧的条件等知识,本题考查的角度和方式新颖,要据相关知识细心解答.




 小红同学依据物质类别和物质中某种元素的化合价回忆了初中化学教材中常见的一些物质,并构建了部分物质间的转化关系坐标图,如图所示(图中“→”表示物质间的转化).已知A、B、C、D含有一种相同的元素,E、F、D含有两种相同的元素,E与H反应生成F且放出大量的热.请回答下列问题:
小红同学依据物质类别和物质中某种元素的化合价回忆了初中化学教材中常见的一些物质,并构建了部分物质间的转化关系坐标图,如图所示(图中“→”表示物质间的转化).已知A、B、C、D含有一种相同的元素,E、F、D含有两种相同的元素,E与H反应生成F且放出大量的热.请回答下列问题: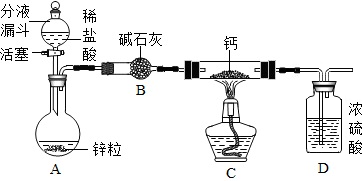
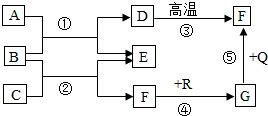 如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色固体(部分反应条件略去),试回答下列问题:
如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,Q、R都是黑色固体(部分反应条件略去),试回答下列问题: