
 探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.分析 (1)活动性强的金属与酸反应剧烈,单位时间内放出的热量多,由此可推知反应现象.
(2)如金属过量,生成氢气的多少就由酸的量决定.
(3)铁与硫酸铜反应时生成的铜会附着在铁的表面,使反应不能彻底进行.
(4)铜在高温下会与氧气反应,烘干后质量增大.
解答 解:(1)从装置图看出,都是密闭的系统,为了观察水被压入漏斗中的量,因此是比较相同时间内镁、铁与稀盐酸反应放出热量的多少的;因为镁和酸反应快,放出的热量多,所以甲装置长颈漏斗中的液面比乙装置中的高;
(2)如金属过量,生成氢气的多少就由酸的量决定,酸的量是相同的,因此放出的氢气质量也相等.
(3)铁与硫酸铜反应时生成的铜会附着在铁的表面,使反应不能彻底进行,所以B方案不能达到目的.
(4)铜在高温下会与氧气反应生成氧化铜,烘干后质量增大,会导致测定的铁的质量分数 偏小.
答案:(1)甲装置长颈漏斗中的液面比乙装置中的高;(2)相等;(3)B;铁未被完全除尽;(4)偏小.
点评 本题从不同角度分析实验过程中的各个环节,从实验目的到实验现象,到实验结果,很有深度,是一道很好的中考题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 需要区分的物质 | 方法一 | 方法二 |
| A | 氧化铁和氧化铜 | 看状态 | 用一氧化碳还原 |
| B | 木炭粉和铁粉 | 观察颜色 | 加稀盐酸 |
| C | 饱和硝酸钾溶液和饱和氢氧化钙溶液 | 升温观察 | 通入二氧化碳 |
| D | 氯化钠和硝酸铵 | 加适量水溶解后测温 度变化 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 烧杯中剩余物质的质量/g | 19.12 | 28.24 | x | 46.48 | 56.48 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
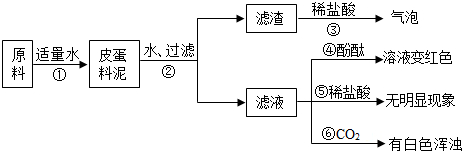
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
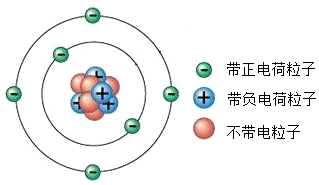 如图为某原子的结构示意图
如图为某原子的结构示意图查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com