
【题目】以工业CuO(含少量FeO)、工业盐酸(含少量稀硫酸)为原料,生产CuCl2·2H2O工艺流程如下。
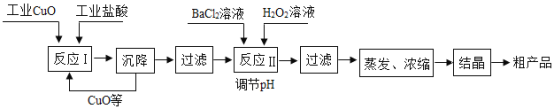
(1)反应Ⅰ中发生了金属氧化物与酸的反应,化学方程式为_____(写一个即可)。
(2)为了加快反应Ⅰ中的反应速度,可以适当加热,但是温度不能过高,原因是__。
(3)反应Ⅱ中发生的3个反应为:
①FeSO4+BaCl2=BaSO4↓+FeCl2;
②CuSO4+BaCl2=BaSO4↓+CuCl2;
③2FeCl2+H2O2+4H2O=2Fe(OH)3↓+4HCl,
其中属于复分解反应的是____(填序号)。
【答案】CuO+2HCl=CuCl2+H2O(或FeO+2HCl=FeCl2+H2O) 盐酸易挥发,温度越高,挥发越快 ①②
【解析】
(1)氧化铜与盐酸反应生成氯化铜和水,氧化亚铜与盐酸反应生成氯化亚铁和水,化学方程式为:CuO+2HCl=CuCl2+H2O(或FeO+2HCl=FeCl2+H2O);
(2)盐酸具有挥发性,温度越高,分子运动速率越快,盐酸挥发越快,将不利于反应的进行,所以需要控制温度,避免盐酸过度挥发;
(3)①、两种反应物相互交换了组分,并有沉淀生成,①属于复分解反应;
②、两种反应物相互交换了组分,并有沉淀生成,②属于复分解反应;
③、反应物为三种,且不是互换组分,虽有沉淀生成,但③不是复分解反应。
故填:①、②。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:
【题目】O2的来源。
(1)实验室制取O2。
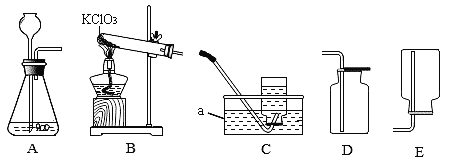
①仪器 a 的名称是_______。
②实验室用KClO3制取O2的化学方程式是___;用酒精灯给试管内固体加热应注意先_____,然后对固体所在部位加热;收集O2可选用的装置是___(填序号)。
③用过氧化氢溶液制取O2时,为避免剧烈反应,可从仪器、试剂、操作等方面进行控制, 结合装置 A 写出一条合理措施_______;反应后剩余药品不要随意丢弃,应________。
(2)自然界生产O2。
①图 1 为自然界中O2的主要来源,其中海洋藻类的光合作用是供氧主力,请将化学方程式补充完整:xCO2+ _______  (CH2O)x+xO2+xH2O。
(CH2O)x+xO2+xH2O。
②图 2 用N2从海水中吹出CO2并用碱液吸收,进一步实验测量海水中无机碳的含量。画出虚线框中的缺损的部分________,最右侧 NaOH 溶液的作用是_______。
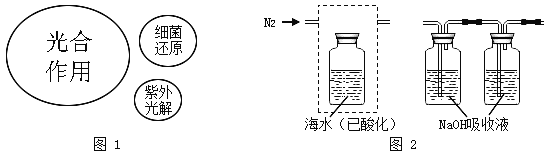
③为保护环境,实验后的海水调节 pH 后重新排回大海,以下说法正确的是______。
A 调节成与排放区域海水相同的 pH
B 调节成弱酸性防止溶解更多的二氧化碳
C 调节成弱碱性吸收更多的二氧化碳,缓解温室效应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用MnO2与浓盐酸反应制备C12,反应的化学方程式为![]() ,反应装置如图1所示。
,反应装置如图1所示。
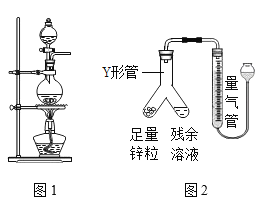
(1)检查装置气密性之后的操作依次是_________(填字母)。
A向烧瓶中加入MnO2粉末
B加热
C向烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余溶液中盐酸的浓度,探究小组同学提出下列实验方案:
①甲同学的方案:利用盐酸和硝酸银反应,化学方程式为______________,利用残余溶液与足量的AgNO3溶液反应,称量生成沉淀的质量,可以测出反应残余溶液中盐酸的浓度。此方案是否可行,请说明原因:______________________。
②乙同学的方案:与足量Zn反应,测量生成的气体体积。实验装置如图2所示(夹持装置已略去)。使Y形管中的残余溶液与锌粒反应的正确操作是将_____________转移到_________________中。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究蜡烛的燃烧做了如下图所示的三个实验。

(1)实验A:取一根小木条平放在蜡烛的火焰中,约1s后取出,与火焰接触的部分,最外侧有明显的烧焦痕迹。该现象说明_____。
(2)实验B:取一个漏斗倒扣在蜡烛火焰上方,将燃着的木条伸到漏斗尖口处,木条熄灭。木条熄灭的原因是_____。
(3)实验C:将燃着的蜡烛放在集气瓶中,密闭,用仪器测得蜡烛由燃烧至熄灭的过程中瓶内氧气的含量。下列说法正确的是_____(填数字序号)。
①蜡烛燃烧需要一定浓度的氧气
②实验开始时,瓶内氧气的体积分数为20%
③蜡烛熄灭后瓶内二氧化碳气体的体积分数为84%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在新型冠状病毒肺炎疫情期间,公共场所需要经常进行消毒。75%的医用酒精和84消毒液能有效消灭病毒。
(1)酒精属于易燃物,使用酒精消毒应远离火源。酒精(C2H5OH)充分燃烧的化学方程式为____。
(2)84消毒液属于含氯消毒剂,这里的氯是指____(填“元素”“原子”或“分子”);84消毒液中的有效成分为次氯酸钠(NaClO),次氯酸钠中氯元素的化合价为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图装置进行可燃物燃烧条件的探究。
已知:白磷着火点为40℃,红磷着火点为240℃。
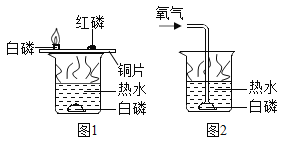
(1)铜片上,白磷发生燃烧,说明铜具有的性质是_____。
(2)验证可燃物燃烧需要与氧气接触,需要对比的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CaCO3广泛存在于自然界,是一种重要的化工原料。某种大理石除主要成分CaCO3外,还含有少量的硫化钙。小李和小明同学用这种大理石和盐酸反应,分别开展以下探究,请你参与探究并回答相关问题。
[查阅资料]
资料一:已知复分解反应![]() 可自发进行。在常温下,测得浓度为a%的下列五种溶液的pH大小情况如下表所示:
可自发进行。在常温下,测得浓度为a%的下列五种溶液的pH大小情况如下表所示:
溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
pH | 小→大 | ||||
表中pH大小情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸。下列反应均能发生,其中不符合该规律的是_____________(填字母代号)。
A![]()
B![]()
C![]()
D![]()
资料二:常见的干燥剂有①浓硫酸、②无水氯化钙、③氢氧化钠固体、④生石灰、⑤五氧化二磷。
[实验探究]小茜同学为了得到纯净的二氧化碳,设计了如图所示装置,请你分析:
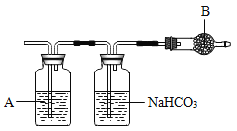
(1)制备的二氧化碳气体中,可能含有的杂质是____________。
(2)上述装置中,A是______________溶液,NaHCO3溶液可以吸收_____________。
(3)上述装置中,B物质不可能是_________(填字每代号)。
A五氧化二磷 B无水氯化钙 C氢氧化钠固体 D生石灰
(4)如果B失效,则得到的二氧化碳质量__________(“偏高”“偏低”或“不受影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下边五环图中的每个环代表初中化学中常见的一种物质,它们分别属于单质、氧化物、酸、碱、盐中的一 种。两环相交表示两者之间能相互反应.下列表述中不符合题意的是
A.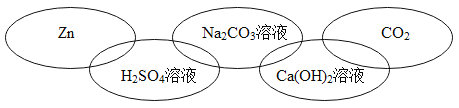 B.
B.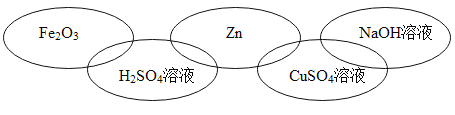
C.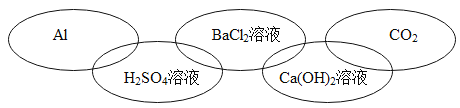 D.
D. 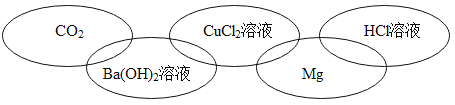
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】扬州,可爱的家乡,美丽的城市: I.世界美食之都——吃在扬州
(1)扬州包子闻名天下:面粉发酵时加入小苏打,在蒸煮过程中其受热分解的化学方程式__。小苏打具有碱性,用 途广泛,但生活中不能用于____(填字母)。
a 除铁锈
b 除油污
c 治疗胃酸过多
d 自制汽水
(2)扬州干丝天下一绝:干丝作为豆制品提供的主要营养成分为____ ,除此还含一定 量的钙,钙元素____ (填“属于”或“不属于”)人体所需微量元素,适量补充钙元素 可以预防____(填字母)。
a 骨质疏松
b 动脉硬化
c 甲状腺肿
d 坏血病
II.世界宜居城市——住在扬州
(3)扬州城市大公园:享受生态之“绿”——绿色植物通过___让城市成为宜居氧吧, 该作用将 ___能转化为化学能。石塔寺千年古银杏顶端安装钢管制成的避雷针,利用了
铁的___性。

(4)扬州公交新能源:感受出行之“绿”——2020 年新能源公交车将超千辆,逐步淘汰传统燃油公交车的意义是_________。 个人绿色出行骑电动车要戴安全头盔,质量好的头盔材质为玻 璃钢。玻璃钢属于__________(填字母)。

a 无机材料
b 合成材料
c 复合材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com