

分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)由于步骤中分离得到蓝色溶液A的操作M是得到蓝色溶液和滤渣(滤渣,过滤得到才叫滤渣),所以为过滤(或者是固体和液体分离操作为过滤),所以操作名称是过滤;
(2)铜可与稀硫酸反应转化为硫酸铜,反应的化学方程式:2Cu+2H2SO4+O2$\stackrel{△}{→}$2CuSO4+2H2O,且为使铜完全反应,加入的稀硫酸是过量的,所以蓝色溶液A中溶质的成分是生成的硫酸铜和剩余的硫酸,对应的化学式为CuSO4、H2SO4;
(3)蓝色溶液中有生成的硫酸铜和剩余的硫酸,而实验目的是回收铜和制备硫酸亚铁,所以应该将铜完全转化为单质,同时除去硫酸,所以为将两者完全除去(所以加入的药品要过量)且不引入新的杂质(所以加入的是铁),所以应该加入过量的铁.所以铁过量的目的是使CuSO4、H2SO4完全反应(说法合理即可);得到的固体C是生成的铜和剩余的铁,而实验目的是得到铜和硫酸亚铁,所以需要加入稀硫酸将铁转化硫酸亚铁然后过滤洗涤干燥得到纯净的铜.所以从固体C中获得纯净的铜,操作(Ⅱ)的具体处理方法是 将所得固体C用稀硫酸酸洗后过滤再洗涤、干燥;
(4)由于“硫酸亚铁晶体的溶解度随着温度升高而增大“和最后得到是硫酸亚铁晶体(FeSO4•7H2O),是带结晶水的化合物,所以整个得到晶体的过程温度不能高,且不能直接蒸干得到固体,所以给定的三步操作的顺序是加热浓缩、冷却结晶、过滤然后进一步用冷水洗涤或者是硫酸亚铁的饱和溶液进行洗涤干燥.所以浅绿色溶液B是经一系列 操作[操作(Ⅰ)]可得硫酸亚铁晶体(FeSO4•7H2O),该系列操作的顺序为 cab、洗涤干燥.
故答案为:
(1)过滤;②CuSO4、H2SO4;③使CuSO4、H2SO4完全反应;将所得固体C用稀硫酸酸洗后过滤再洗涤、干燥;④c→a→b
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | He、Ne、Ar | B. | Na+、Mg2+、Al3+ | C. | NH${\;}_{4}^{+}$、OH-、F- | D. | HF、H2O、NH3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “对乙酰氨基酚”由碳、氢、氮、氧四种元素组成 | |
| B. | “对乙酰氨基酚”是有机物 | |
| C. | “对乙酰氨基酚”分子中碳、氢、氮、氧元素质量比是8:9:1:2 | |
| D. | “对乙酰氨基酚”中碳元素的质量分数约为63.6% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
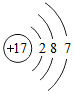 如图是某原子的结构示意图.下列关于该原子的说法不正确的是( )
如图是某原子的结构示意图.下列关于该原子的说法不正确的是( )| A. | 属于金属元素原子 | B. | 最外层电子数为 7 | ||
| C. | 反应过程中容易得到电子 | D. | 有 3 个电子层 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 钛酸亚铁(FeTiO3)中钛元素化合价为+3价 | |
| B. | ①中反应是氧化还原反应 | |
| C. | ③中氩气(Ar)作反应物 | |
| D. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为14:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com