
| A£® | +1 | B£® | +2 | C£® | +3 | D£® | +4 |
·ÖĪö øł¾ŻŌŚ»ÆŗĻĪļÖŠÕżøŗ»ÆŗĻ¼Ū“śŹżŗĶĪŖĮć£¬½įŗĻŃĒĻõĖįÄĘ£ØNaNO2£©µÄ»ÆѧŹ½½ųŠŠ½ā“š±¾Ģā£®
½ā“š ½ā£ŗÄĘŌŖĖŲĻŌ+1£¬ŃõŌŖĖŲĻŌ-2£¬ÉčŃĒĻõĖįÄĘÖŠµŖŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒx£¬
øł¾ŻŌŚ»ÆŗĻĪļÖŠÕżøŗ»ÆŗĻ¼Ū“śŹżŗĶĪŖĮć£¬
æÉµĆ£ŗ£Ø+1£©+x+£Ø-2£©”Į2=0£¬
Ōņx=+3£®
¹ŹŃ”£ŗC£®
µćĘĄ ±¾ĢāÄŃ¶Č²»“ó£¬æ¼²éѧɜĄūÓĆ»ÆŗĻ¼ŪµÄŌŌņ¼ĘĖćÖø¶ØŌŖĖŲµÄ»ÆŗĻ¼ŪµÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO32- K+ Cl- Ca2+ | B£® | K+ NO3- Na+ OH- | ||
| C£® | H+ Ba2+ Cl- SO42- | D£® | K+ OH- SO42- Cu2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 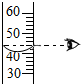 ĮæČ”ŅŗĢå | B£® | 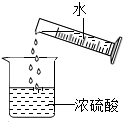 Ļ”ŹĶÅØĮņĖį | C£® | 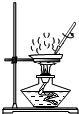 Õō·¢Ź³ŃĪĖ® | D£® | 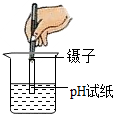 ²āČÜŅŗpH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
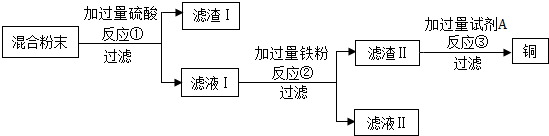
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| “ĪŹż | 1 | 2 | 3 | 4 |
| ¼ÓČėĻ”ĮņĖįÖŹĮæ/g | 70.0 | 70.0 | 70.0 | 70.0 |
| Ź£Óą¹ĢĢåÖŹĮæ/g | 13.6 | 11.2 | 8.8 | 7.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŃĪČÜŅŗ | CaCl2ČÜŅŗ | Na2CO3ČÜŅŗ | NaClČÜŅŗ |
| pH | µČÓŚ7 | “óÓŚ7 | µČÓŚ7 |
| ŹµŃé²½Öč | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ²½ÖčŅ»£ŗȔɣĮæѳʷӌŹŌ¹ÜÖŠ£¬ ¼ÓŹŹĮæĖ®Õńµ“ŗóČ«²æČܽā£¬µĪ ČėCaCl2ČÜŅŗÖĮ¹żĮ棬³ä·Ö·“ Ó¦ŗ󣬾²ÖĆ£® | °×É«³Įµķ | ѳʷ֊Ņ»¶Øŗ¬ÓŠNa2CO3 £ØĢī»ÆѧŹ½£© |
| ²½ÖčŅ»£ŗČ”²½ÖčŅ»³ä·Ö·“Ó¦ŗó µÄÉŁĮæÉĻ²ćĒåŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ ČėĪŽÉ«·ÓĢŖŹŌŅŗ | ½įŗĻĮ½²½ŹµŃéµĆ³ö ²ĀĻėŅ»³ÉĮ¢£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
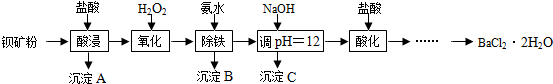
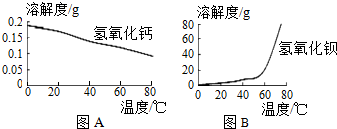
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Éś»īÖŠ¼ūµ½µÄ”°¼ÓµāŹ³ŃĪ”±”¢”°øßøĘÅ£ÄĢ”±ÖŠµÄ”°µā”¢øĘ”±Ó¦Ąķ½āĪŖŌŖĖŲ | |
| B£® | ”°Ē½ÄŚæŖ»ØĒ½ĶāĻć”±ĖµĆ÷·Ö×ÓŹĒ²»¶ĻŌĖ¶ÆµÄ | |
| C£® | Ė®ŌŚĶصēµÄĢõ¼žĻĀÄÜÉś³ÉĒāĘųŗĶŃõĘų£¬ĖµĆ÷Ė®ŹĒÓÉĒāĘųŗĶŃõĘų×é³ÉµÄ | |
| D£® | Ė®ŗĶ¹żŃõ»ÆĒā»ÆѧŠŌÖŹ²»Ķ¬ŹĒŅņĪŖ·Ö×Ó¹¹³É²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com