

分析 (1)铁在氧气中燃烧时放出大量的热,生成的四氧化三铁的温度很高,容易溅落从而把集气瓶炸裂.所以实验时应该在集气瓶底部放入少量的水或铺一层细沙;
(2)根据红磷在空气中燃烧产生大量白烟,放出大量的热;红磷在空气中燃烧是与空气中的氧气反应,会消耗空气中的氧气,冷却后空气的体积会减少,减少的就是空气中氧气的体积解答;
(3)根据俯视读数时读数大于实际数分析回答.
解答 解:(1)铁丝在氧气中燃烧,集气瓶底部要预先放少量的水或铺一层细沙,目的是防止生成物熔化溅落下来炸裂集气瓶.铁在氧气中燃烧生成四氧化三铁,方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(2)B利用红磷燃烧进行空气中氧气含量,能观察到的主要现象是:红磷在空气中燃烧产生大量的白烟.红磷在空气中燃烧是与空气中的氧气反应,会消耗空气中的氧气,冷却后空气的体积会减少,因此打开止水夹时,水会进入集气瓶,约占集气瓶容积的$\frac{1}{5}$;
(3)由图示可知是俯视读数,量取的水偏少,该操作将导致所配溶液溶质质量分数偏大.
故答案为:(1)放少量的水或铺一层细沙;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4(2)产生大量的白烟,水会进入集气瓶,约占集气瓶容积的$\frac{1}{5}$;(3)偏大.
点评 本题的难度不大,解答本题的关键是要了解实验的注意事项、实验的现象等知识.


 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
| B | N2 | O2 | 将混合气体通过灼热的铜网 |
| C | CO2 | CO | 将混合气体点燃 |
| D | Cu(NO3)2溶液 | AgNO3 | 加入过量的铜粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 组别 | 1 | 2 | 3 | 4 | 5 |
| 进入集气瓶中水的体积/mL | 21 | 19 | 22 | 15 | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
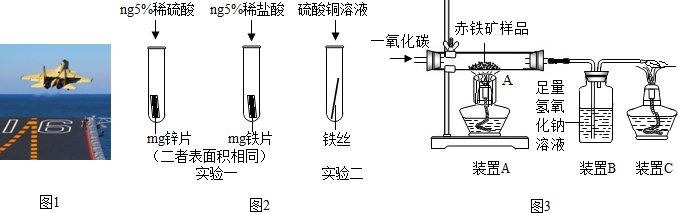
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com